题目内容
11.某无色透明溶液,在pH=0和pH=14的条件下都能大量共存的是( )| A. | Fe2+、K+、SO42ˉ、NO3ˉ | B. | Mg2+、NH4+、SO42-、Clˉ | ||
| C. | Na+、K+、SO42ˉ、NO3ˉ | D. | Ba2+、Na+、CO32-、NO3ˉ |
分析 pH=0的溶液中含大量的氢离子,pH=14的溶液中含大量的氢氧根离子,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.Fe2+为浅绿色,与无色不符,故A不选;
B.碱溶液中不能大量存在Mg2+、NH4+,故B不选;
C.酸、碱溶液中该组离子之间均不反应,可大量共存,且离子均为无色,故C选;
D.酸溶液中不能大量存在CO32-,且CO32-、Ba2+结合生成沉淀,不能共存,故D不选;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息、常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
相关题目
19.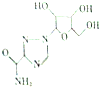 利巴韦林适用于拉萨热、幼儿呼吸道合胞病毒肺炎、带状咆疹等,其结构简式如图,下列关于利巴韦林的说法错误的是( )
利巴韦林适用于拉萨热、幼儿呼吸道合胞病毒肺炎、带状咆疹等,其结构简式如图,下列关于利巴韦林的说法错误的是( )
 利巴韦林适用于拉萨热、幼儿呼吸道合胞病毒肺炎、带状咆疹等,其结构简式如图,下列关于利巴韦林的说法错误的是( )
利巴韦林适用于拉萨热、幼儿呼吸道合胞病毒肺炎、带状咆疹等,其结构简式如图,下列关于利巴韦林的说法错误的是( )| A. | 分子式为C8H12N4O3 | B. | 能使紫色石蕊试液变红 | ||
| C. | 可以发生酯化反应 | D. | 可以与H2发生加成反应 |
2.元素的性质随着原子序数的递增呈现周期性变化的主要原因是( )
| A. | 元素原子的核外电子排布呈周期性变化 | |
| B. | 元素的化合价呈周期性变化 | |
| C. | 元素原子的金属性、非金属性呈周期性变化 | |
| D. | 元素的原子半径呈周期性变化 |
19.室温时,下列混合溶液的pH一定小于7的是( )
| A. | pH=3的盐酸和pH=11的氨水等体积混合 | |
| B. | 0.1mol/L的盐酸和0.1mol/L的氢氧化钡溶液等体积混合 | |
| C. | pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 | |
| D. | pH=3的硫酸和pH=11的氨水等体积混合 |
6.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 氧化钙溶于水 | B. | 铁粉溶于稀硫酸 | ||
| C. | 盐酸与氢氧化钠反应 | D. | 氢氧化钡晶体与氯化铵晶体混合 |
16.下列各组的电极材料和电解液,不能组成原电池的是( )
| A. | 铜片、铜片、稀硫酸 | B. | 铜片、石墨棒、硝酸银溶液 | ||
| C. | 锌片、铜片、稀硫酸 | D. | 铜片、银片、FeCl3溶液 |
3.A元素原子最外层电子数是次外层电子数的3倍,B元素原子最外层电子数是次外层电子数的一半,则A、B元素( )
| A. | 一定是第二周期元素 | B. | 一定是同一主族元素 | ||
| C. | 可能是第二、三周期元素 | D. | A、B只能形成化合物B2A |
20.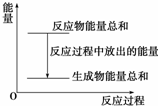 对于敞口容器中的化学反应:Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g),下列叙述中不正确的是( )
对于敞口容器中的化学反应:Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g),下列叙述中不正确的是( )
 对于敞口容器中的化学反应:Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g),下列叙述中不正确的是( )
对于敞口容器中的化学反应:Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g),下列叙述中不正确的是( )| A. | Zn和H2SO4的总能量大于ZnSO4和H2的总能量 | |
| B. | 反应过程中能量关系可用如图表示 | |
| C. | 若将该反应设计成原电池,则Zn为负极 | |
| D. | 若将该反应设计成原电池,当有32.5g锌溶解时,正极放出11.2 L气体 |