题目内容
11.氨气是重要的化工原料,可以用来制备硝酸以及各种化肥产品.(1)氨分子的电子式为
 .
.(2)写出一水合氨的电离方程式NH3•H2O?NH4++OH-;现在在10ml0.1mol/L的一水合氨溶液中滴加0.1mol/L的盐酸,若要使在常温下混合溶液的pH=7,那么需要滴加盐酸溶液的体积小于10ml(选填大于、等于、小于)
(3)用两根玻璃棒,一根蘸取浓氨水,一根蘸取浓硫酸,当两根玻璃棒靠近时,出现的现象是有白烟生成;该反应的化学方程式为HCl+NH3=NH4Cl.
分析 (1)氨气分子中氮原子最外层达到8电子稳定结构;
(2)一水合氨为弱电解质,部分电离,用可逆号;若加入的盐酸能将一水合氨完全中和,则所得的氯化铵溶液水解显酸性;
(3)浓盐酸和浓氨水均易挥发,挥发出HCl和NH3,两者相遇生成氯化铵为白烟,据此分析.
解答 解:(1)氨气分子中氮原子最外层达到8电子稳定结构,漏掉了氮原子的一对孤电子对,氨气的电子式为 ,故答案为:
,故答案为: ;
;
(2)一水合氨为弱电解质,部分电离,电离方程式;NH3•H2O?NH4++OH-;若加入的盐酸能将一水合氨完全中和,则所得的氯化铵溶液水解显酸性,故若要使在常温下混合溶液的pH=7,那么需要滴加盐酸溶液体积小于10mL.
故答案为:NH3•H2O?NH4++OH-;小于;
(3)浓盐酸和浓氨水均易挥发,挥发出HCl和NH3,两者相遇生成氯化铵为白烟,化学方程式为:HCl+NH3=NH4Cl,故答案为:有白烟生成;HCl+NH3=NH4Cl.
点评 本题考查了常见物质的电子式的书写和弱电解质的电离方程式等的书写,应注意的是弱电解质的电离用可逆号,强电解质的电离用等号.

练习册系列答案
相关题目
2.有下列物质:①石墨 ②铜丝 ③氧气 ④二氧化碳 ⑤NaCl固体 ⑥稀H2SO4 ⑦水 ⑧硫酸钡 ⑨金刚石,以下组合正确的是( )
| A. | 能导电的有①②⑤⑥ | |
| B. | 属于电解质的有⑤⑦⑧ | |
| C. | 属于强电解质的有⑤⑥⑧ | |
| D. | 既不属于电解质又不属于非电解质的有①②③④ |
19.下列叙述正确的是( )
| A. | KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | |
| B. | 煤的干馏和气化都是物理变化 | |
| C. | 氯水、氨水、王水是混合物,水银、水玻璃是纯净物 | |
| D. | 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
6.向35.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体完全反应,生成NO 和Cu(NO3)2.在所得溶液中加入1.0mol/L 的NaOH溶液1.3L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为49g.下列有关说法正确的是( )
| A. | Cu与Cu2O 的物质的量之比为2:1 | |
| B. | 硝酸的物质的量浓度为2.6mol/L | |
| C. | 产生的NO在标准状况下的体积为4.48L | |
| D. | Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
16.下列说法正确的是( )
| A. | 可用焰色反应来证明某试样中是否含有钠元素 | |
| B. | 至少用二种试剂通过化学反应能区别开硫酸铵、硫酸钾、氯化铵 | |
| C. | 配制物质的量溶液定容时,加水超过刻度线,用胶头滴管吸出 | |
| D. | 粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶 |
3.现有部分短周期主族元素的性质或原子结构如表:
(1)写出A单质与水反应的化学方程式:2Na+2H2O=2NaOH+H2↑.
(2)B元素气态氢化物的电子式是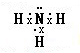 ,该氢化物溶于水,水溶液呈碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-.
,该氢化物溶于水,水溶液呈碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-.
(3)探寻物质的性质差异性是学习的重要方法之-.A、B、C、D、E五种元素的单质中化学性质明显不同于其它四种单质的是Na(用化学式表示),理由钠是金属单质,其它的是非金属单质.
(4)B、D两元素非金属性较强的是(写元素符号)N.写出证明这一结论的一个实验事实硝酸的酸性比碳酸强.
| 元素编号 | 元素性质或原子结构 |
| A | 常温下单质能与水剧烈反应,所得溶液呈强碱性 |
| B | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| C | 第三周期元素的原子中半径最小 |
| D | D的一种同位素可测定文物年代 |
| E | 次外层电子数比最外层电子数多2个 |
(2)B元素气态氢化物的电子式是
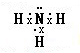 ,该氢化物溶于水,水溶液呈碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-.
,该氢化物溶于水,水溶液呈碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-.(3)探寻物质的性质差异性是学习的重要方法之-.A、B、C、D、E五种元素的单质中化学性质明显不同于其它四种单质的是Na(用化学式表示),理由钠是金属单质,其它的是非金属单质.
(4)B、D两元素非金属性较强的是(写元素符号)N.写出证明这一结论的一个实验事实硝酸的酸性比碳酸强.
3.下列化学用语正确的是( )
| A. | CO2的电子式: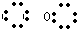 | B. | Mg2+的结构示意图: | ||
| C. | Na2O的电子式:Na+2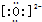 | D. | N2的结构式:N≡N |