题目内容
某温度下,将0.10mol CH3COOH溶于水配成1L溶液,实验测得已电离的醋酸分子占原有醋酸分子总数的1.3%,若水的电离忽略不计,醋酸电离对醋酸分子浓度的影响忽略不计,求得该温度下CH3COOH的电离平衡常数K=1.7×10-5.向该溶液中再加入 mol CH3COONa可使溶液的pH约为4.(溶液体积变化忽略不计)
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:根据K=
来计算;并根据溶液pH值的计算方法进行计算.
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
解答:
解:K=
=
=1.7×10-5,溶液中pH=pKa-lg
=-lg1.7×10-5-lg
=4,所以c(CH3COONa)=1.7×10-2mol/L,则n(CH3COONa)=1.7×10-2mol/L×1L=1.7×10-2mol,故答案为:1.7×10-2.
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
| (0.1mol/L×1.3%)2 |
| 0.1molL×(1-1.3%) |
| c(CH3COOH) |
| c(CH3COONa) |
| 0.1 |
| c(CH3COONa) |
点评:本题考查了弱电解质的电离,难点是计算醋酸钠的物质的量,明确溶液的pH计算方法是解本题关键,难度中等.

练习册系列答案
相关题目
下列分子中,电子总数最少的是( )
| A、H2S |
| B、O2 |
| C、CO |
| D、NO |
除去CuSO4溶液中含有的Fe2(SO4)3杂质,最佳的方法是加入( )
| A、CuO |
| B、H2O2 |
| C、NH3?H2O |
| D、NaOH |
 洋蓟在国际市场上属高档蔬菜,以良好的保健功能和药用价值被冠以“蔬之皇”的美称,从洋蓟提取的洋蓟素结构如图,请回答下列问题
洋蓟在国际市场上属高档蔬菜,以良好的保健功能和药用价值被冠以“蔬之皇”的美称,从洋蓟提取的洋蓟素结构如图,请回答下列问题 +A
+A
 元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系.
元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系. A、B、C、D、E、F均为周期表中前四周期的元素.请按要求回答下列问题.
A、B、C、D、E、F均为周期表中前四周期的元素.请按要求回答下列问题.
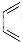 +
+ →G(抗病毒药阿昔洛韦中间体),G的结构简式为:
→G(抗病毒药阿昔洛韦中间体),G的结构简式为: )是一种重要的工业原料,某研究性学习小组的同学拟用下列装置制取高纯度的苯甲酸甲酯.
)是一种重要的工业原料,某研究性学习小组的同学拟用下列装置制取高纯度的苯甲酸甲酯.