题目内容
4.写出下列反应的方程式:(1)1-氯丙烷与NaOH溶液混合加热:CH3CH2CH2Cl+NaOH$→_{△}^{H_{2}O}$CH3CH2CH2OH+NaCl;
(2)2-溴丙烷与NaOH醇溶液混合加热:CH3CHBrCH3+NaOH $→_{△}^{醇}$CH3CH=CH2↑+NaBr+H2O;
(3)实验室制备乙炔的反应:CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(4)苯的硝化反应:
 .
.
分析 (1)1-氯丙烷与NaOH溶液混合加热发生取代反应或水解反应生成1-丙醇和NaCl;
(2)2-溴丙烷与NaOH醇溶液混合加热发生消去反应生成2-丙醇、NaBr和H2O;
(3)实验室制备乙炔用碳化钙和水反应制取;
(4)苯和浓硝酸在浓硫酸作催化剂、50℃~60℃加热条件下发生取代反应生成硝基苯.
解答 解:(1)1-氯丙烷与NaOH溶液混合加热发生取代反应或水解反应生成1-丙醇和NaCl,反应方程式为CH3CH2CH2Cl+NaOH$→_{△}^{H_{2}O}$CH3CH2CH2OH+NaCl,
故答案为:CH3CH2CH2Cl+NaOH$→_{△}^{H_{2}O}$CH3CH2CH2OH+NaCl;
(2)2-溴丙烷与NaOH醇溶液混合加热发生消去反应生成2-丙醇、NaBr和H2O,反应方程式为CH3CHBrCH3+NaOH $→_{△}^{醇}$CH3CH=CH2↑+NaBr+H2O,
故答案为:CH3CHBrCH3+NaOH $→_{△}^{醇}$CH3CH=CH2↑+NaBr+H2O;
(3)实验室制备乙炔用碳化钙和水反应制取,反应方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑,故答案为:CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(4)苯和浓硝酸在浓硫酸作催化剂、50℃~60℃加热条件下发生取代反应生成硝基苯,反应方程式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机化学反应方程式的书写,为高频考点,根据反应物、生成物及反应条件书写方程式,知道常见反应类型及反应条件、有机物官能团及其性质,注意硝基的书写方法,为易错点.

练习册系列答案
相关题目
14.我国科学家成功地研制出一种长期依赖进口、价格昂贵的物质18O2.下列说法正确的是( )
| A. | 它是O3的一种同素异形体 | B. | 它是16O2的同分异构体 | ||
| C. | 18O2与16O2互为同位素 | D. | 1mol18O2分子中含有20mol电子 |
15.LED系列产品是一类新型节能产品.图甲是NaBH4/H2O2燃料电池,图乙是LED发光二极管的装置示意图.下列叙述错误的是( )
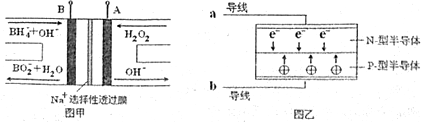

| A. | 电池A极区的电极反应式为:H2O2+2e-=2OH- | |
| B. | 电池放电过程中,Na+从负极区向正极区移动 | |
| C. | 每有1mol NaBH4参加反应转移电子数为4NA | |
| D. | 要使LED发光二极管正常发光,图乙中的导线a应与图甲中的B极相连 |
19.己知:Mn(s)+O2(g)═MnO2(s)△Hl
S(s)+O2(g)═SO2(g)△H2
Mn(s)+S(s)+2O2(g)═MnSO4(s)△H3
则下列表述正确的是( )
S(s)+O2(g)═SO2(g)△H2
Mn(s)+S(s)+2O2(g)═MnSO4(s)△H3
则下列表述正确的是( )
| A. | △H2>0 | |
| B. | △H3>△H1 | |
| C. | Mn+SO2═MnO2+S△H=△H2-△H1 | |
| D. | MnO2(s)+SO2(g)═MnSO4(s)△H═△H3-△H2-△H1 |
17.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 2.3克金属钠在干燥空气中被氧化成氧化物时失去的电子数目为0.1NA | |
| B. | 18克水所含的质子数目为NA | |
| C. | 在常温常压下,11.2升氯气所含的分子数目为0.5NA | |
| D. | 32克臭氧所含的原子数目为NA |
 在298K时,1mol C2H5OH在氧气中完全燃烧生成二氧化碳和液态水放出热量1366.8kJ.
在298K时,1mol C2H5OH在氧气中完全燃烧生成二氧化碳和液态水放出热量1366.8kJ.
 ;反应类型酯化反应会取代反应;
;反应类型酯化反应会取代反应;