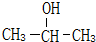题目内容
8.如果一个反应△H-T△S值小于零,则此反应( )| A. | 能自发进行 | B. | 是放热反应 | C. | 不能自发进行 | D. | 处于平衡状态 |
分析 根据△H-T△S判断反应自发性,当△H-T△S<0能自发,当△H-T△S>0不能自发,当△H-T△S=0处于平衡状态.
解答 解:根据△H-T△S判断反应自发性,当△H-T△S<0能自发,当△H-T△S>0不能自发,当△H-T△S=0处于平衡状态,故选:A.
点评 本题考查了反应自发性的判断,题目难度不大,侧重基本概念的考查,注意基础知识的积累.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
19.下列变化中生成物的总能量大于反应物的总能量的是( )
| A. | 镁与稀盐酸反应 | B. | CO燃烧生成CO2 | ||
| C. | 氢氧化钡晶体与氯化铵晶体反应 | D. | 生石灰溶于水 |
16.以下物质间的每步转化通过一步反应能实现的是( )
| A. | Al→Al2O3→Al(OH)3→Na[Al(OH)4] | B. | N2→NO→NO2→HNO3 | ||
| C. | Si→SiO2→H2SiO3→Na2SiO3 | D. | S→SO3→H2SO4→MgSO4 |
13.实验测得常温下0.1mol/L某一元酸HA溶液的pH不等于l,0.1mol/L某一元碱BOH溶液里:$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12.将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
| A. | c(A-)>c(B+)>c(H+)>c(OH-) | B. | c(B+)>c(A-)>c(OH-)>c(H+) | ||
| C. | c(B+)+c (H+)>c(A-)+c(OH-) | D. | c(B+)>c(A-)>c(H+)>c(OH-) |
20.下列说法正确的是( )
| A. | 一定温度下,10mL 0.50mol•L-1NH4Cl溶液与20mL 0.25mol•L-1NH4C1溶液含NH4+物质的量相同 | |
| B. | 25℃时,将a mo1•L-l氨水与0.01 moI•L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示反应完全时NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
| C. | 一定温度下,已知0.1 mol•L-1 的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,加少量烧碱溶液可使溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$值增大 | |
| D. | 等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA>HB |
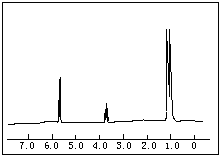 (1)已知1-丙醇和2-丙醇的结构简式如图:
(1)已知1-丙醇和2-丙醇的结构简式如图: