题目内容
下列有关说法正确的是(NA为阿伏加德罗常数)( )
| A、1.00molNaCl中含有NA个NaCl分子 |
| B、欲配制1.00L,1.00mol.L-1的NaCl溶液,可将58.5gNaCl溶于 1.00L水 |
| C、1.12L Cl2含有1.7NA个质子 |
| D、1molCl2与足量的铁反应,转移的电子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、氯化钠是离子晶体,不含分子;
B、将58.5gNaCl溶于 1.00L水后,溶液体积大于1L;
C、氯气所处的状态不明确;
D、根据反应后氯元素的价态来分析.
B、将58.5gNaCl溶于 1.00L水后,溶液体积大于1L;
C、氯气所处的状态不明确;
D、根据反应后氯元素的价态来分析.
解答:
解:A、氯化钠是离子晶体,不含分子,故A错误;
B、溶液的体积不等同于溶剂的体积,当将58.5gNaCl溶于 1.00L水后,溶液体积大于1L,故所配溶液的浓度小于1.00mol/L,故B错误;
C、氯气所处的状态不明确,不一定是标况,故物质的量不一定是0.5mol,故C错误;
D、反应后氯元素的价态为-1价,故1mol氯气转移2mol电子,故D正确.
故选D.
B、溶液的体积不等同于溶剂的体积,当将58.5gNaCl溶于 1.00L水后,溶液体积大于1L,故所配溶液的浓度小于1.00mol/L,故B错误;
C、氯气所处的状态不明确,不一定是标况,故物质的量不一定是0.5mol,故C错误;
D、反应后氯元素的价态为-1价,故1mol氯气转移2mol电子,故D正确.
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
下列有关化学用语的表示正确的是( )
A、N2的电子式: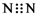 | ||
B、CH4的比例模型: | ||
C、中子数为45的溴原子:
| ||
D、对羟基苯甲酸的结构简式: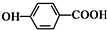 |
当光束通过下列分散系时,可能产生丁达尔效应的是( )
| A、NaHCO3溶液 |
| B、蔗糖溶液 |
| C、CuSO4溶液 |
| D、Fe(OH)3胶体 |
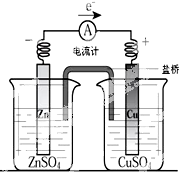 用铜片、锌片、CuSO4溶液、ZnSO4溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池.以下有关该原电池的叙述正确的是( )
用铜片、锌片、CuSO4溶液、ZnSO4溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池.以下有关该原电池的叙述正确的是( ) 如图所示,已知:
如图所示,已知: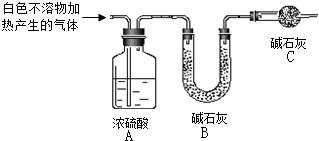 资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学通过如下实验探究反应原理并验证产物.
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学通过如下实验探究反应原理并验证产物.