题目内容
将Mg、Cu组成的混合物26.4g,投入到适量的稀硝酸中,固体完全溶解,收集到标准状况下的NO气体8.96L,向反应后的溶液中加入过量的5mol/L的NaOH溶液300mL,金属离子完全沉淀.则形成沉淀的质量是( )
| A、32.8g |
| B、46.8g |
| C、53.6g |
| D、63.8g |
考点:有关混合物反应的计算
专题:
分析:Mg、Cu在反应中失去电子,最终生成Mg(OH)2、Cu(OH)2,根据电荷守恒可知,金属失去电子的物质的量等于生成沉淀需要氢氧根离子的物质的量,根据生成NO的气体的物质的量,利用电子转移守恒计算转移电子的物质的量,最终生成沉淀的质量=金属的质量+氢氧根离子的质量.
解答:
解:根据电子转移守恒可知,Mg、Cu生成8.96LNO转移的电子为:
×(5-2)=1.2mol,
Mg、Cu在反应中失去电子,最终生成Mg(OH)2、Cu(OH)2,根据电荷守恒可知,生成沉淀需要氢氧根离子的物质的量等于Mg、Cu失去电子的物质的量,所以反应后生成沉淀的质量为:26.4g+1.2mol×17g/mol=46.8g,
故选B.
| 8.96L |
| 22.4L/mol |
Mg、Cu在反应中失去电子,最终生成Mg(OH)2、Cu(OH)2,根据电荷守恒可知,生成沉淀需要氢氧根离子的物质的量等于Mg、Cu失去电子的物质的量,所以反应后生成沉淀的质量为:26.4g+1.2mol×17g/mol=46.8g,
故选B.
点评:本题考查混合物的计算、氧化还原反应计算,题目难度中等,侧重对解题方法技巧与学生综合能力的考查,注意利用电子转移的数目和氢氧根离子之间的关系解答.

练习册系列答案
相关题目
下列说法正确的是( )
| A、已知:N2(g)+2O2(g)=2NO2(g)△H=+68kJ?mol-12C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1C(s)+O2(g)=CO2(g)△H=-393.5kJ?mol-1则4CO(g)+2NO2(g)=4CO2(g)+N2(g)△H=+1200kJ?mol-1 | ||||||||||||
| B、由H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ?mol-1,则向含0.1 mol HCl的盐酸中加入4.0 gNaOH固体,放出热量等于5.73 kJ | ||||||||||||
C、通常人们把拆开1 mol气态物质中某种共价键需要吸收的能量看成该共价键的键能
| ||||||||||||
| D、NH4HCO3(s)═NH3 (g)+H2O(g)+CO2(g)△H=+185.57 kJ?mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
现在铁与另一种金属组成的混合物1.2g,与足量稀硫酸反应生成H2 0.1g,则混合物中的另一种金属可能是( )
| A、Mg | B、Al | C、Zn | D、Cu |
CH3COOH溶液与NaOH溶液反应,若反应后溶液的pH为7,那么( )
| A、CH3COOH与NaOH的质量相等 |
| B、CH3COOH与NaOH的物质的量相等 |
| C、NaOH过量 |
| D、CH3COOH过量 |
一定温度下,在密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法不正确的是( )
| 物质 | X | Y | Z | W |
| 初始浓度/mol?L-1 | 0.5 | 0.5 | 0 | 0 |
| 平衡浓度/mol?L-1 | 0.1 | 0.1 | 0.4 | 0.4 |
| A、反应达到平衡时,X的体积分数为10% |
| B、该温度下反应的平衡常数K=16 |
| C、保持温度不变增大压强,反应速率加快,平衡向正反应方向移动 |
| D、若X、Y的初始浓度均为0.8 mol?L-1,相同条件下达到平衡,W的浓度为0.64 mol?L-1 |
下列措施不符合节能减排的是( )
| A、大力发展火力发电,解决电力紧张问题 |
| B、发展低碳经济、循环经济,推广利用太阳能、风能 |
| C、用石灰对煤燃烧后形成的烟气脱硫,并回收石膏 |
| D、用杂草、生活垃圾及有机废弃物在沼气池中发酵产生沼气,作家庭燃气 |
 某学生设计如下实验装置利用氯气与消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
某学生设计如下实验装置利用氯气与消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题: 用
用 通过以下路线可合成(G):
通过以下路线可合成(G):
 ,请写出以甲醇和A为原料制备
,请写出以甲醇和A为原料制备 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).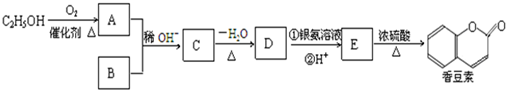
 (R、R′为烃基)
(R、R′为烃基)