题目内容
9.下列关于能源的说法不正确的是( )| A. | 植物通过光合作用,将太阳能转化为生物质能 | |
| B. | 在农村推广建造沼气池,是对生物质能的有效利用 | |
| C. | 天然气的主要成分是甲烷,是一种可再生的清洁能源 | |
| D. | 氢能是重要的清洁能源,在蓝绿藻、微生物和太阳光作用下使水分解制氢是目前科学家研究的新方法之一 |
分析 A.绿色植物具有光合作用,光合作用将太阳能转化为生物质能;
B.生物质发酵可生成甲烷;
C.甲烷不可再生;
D.在蓝绿藻、微生物和太阳光作用下使水分解制氢,可制备清洁能源.
解答 解:A.绿色植物具有光合作用,光合作用将太阳能转化为生物质能,故A正确;
B.生物质发酵可生成甲烷,则在农村推广建造沼气池,是对生物质能的有效利用,故B正确;
C.煤、石油、天然气属于化石燃料,它们都是不可再生能源,故C错误;
D.在蓝绿藻、微生物和太阳光作用下使水分解制氢,可制备清洁能源,故D正确.
故选C.
点评 本题考查化学反应与能量,为高频考点,侧重于化学与生活、环境的考查,有利于培养学习的良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
7.元素①~⑩在周期表中的位置如表所示,试回答下列问题.
(1)上述10种元素中,化学性质最不活泼的是Ar(填元素符号,下同);与水反应最激烈的金属元素是K.
(2)元素 ②的气态氢化物的分子式是NH3;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是HClO4(填化学式).
(3)用电子式表示元素③与④形成1:2型化合物的形成过程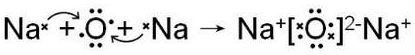 .
.
(4)①②⑤元素的原子半径由小到大的顺序为N、C、Mg(用元素符号表示);③⑦⑩元素的气态氢化物的稳定性由强到弱的顺序为H2O、HCl、HBr(用氢化物的化学式表示).
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)元素 ②的气态氢化物的分子式是NH3;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是HClO4(填化学式).
(3)用电子式表示元素③与④形成1:2型化合物的形成过程
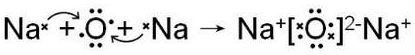 .
.(4)①②⑤元素的原子半径由小到大的顺序为N、C、Mg(用元素符号表示);③⑦⑩元素的气态氢化物的稳定性由强到弱的顺序为H2O、HCl、HBr(用氢化物的化学式表示).
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
20.下列实验方案能达到实验目的是( )
| 选项 | 实验H的 | 实验方案 |
| A | 证明Mg(OH)2沉淀可以转化为 Fe(OH)3 | 向2mL1mol/LNaOH溶液中先加入3滴1mol/LMgCl2溶液,再加入3滴1mol/LFeCl3溶液 |
| B | 比较氯和碳的非属性强弱 | 将盐酸滴入碳酸氢钠溶液中 |
| C | 验证电解饱和食盐水阳极有氯气生成 | 以铁为电极电解饱和食盐水,并将阳极生成的气体通入淀粉-KI溶液 |
| D | 比较铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合溶液 |
| A. | A | B. | B | C. | C | D. | D |
17.下列实验方案能达到实验目的是( )
| 选项 | 实验方案 | 实验目的或结论 |
| A | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 可证明氧化性:H2O2比Fe3+强 |
| B | 向1mL 1%的NaOH溶液中加入2mL2%的CuSO4溶液,振荡,再加入0.5mL有机物Y,加热,未出现砖红色沉淀 | 说明Y中不含醛基 |
| C | 取a g铝箔与足量氢氧化钠溶液充分反应,逸出的气体通过浓硫酸后,测其体积为V L(已转化为标准状况下) | 测定铝箔中氧化铝的含量 |
| D | 比较不同反应的反应热数据大小 | 从而判断反应速率的大小 |
| A. | A | B. | B | C. | C | D. | D |
4.化学与生产、生活、社会发展等息息相关.下列说法正确的是( )
| A. | 利用植物油的氧化反应可获得人造脂肪 | |
| B. | 干馏煤可以得到甲烷、苯和氨等重要化工原料 | |
| C. | 工业生产玻璃、水泥和陶瓷,均需用石灰石作原料 | |
| D. | 明矾和“84”消毒液均可用于自来水的杀菌消毒 |
14.下列有关化学用语表示正确的是( )
| A. | 中子数为14的铝原子:${\;}_{13}^{14}$Al | B. | 次氯酸的电子式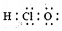 | ||
| C. | O2-的结构示意图: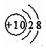 | D. | 聚四氟乙烯的结构简式: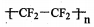 |
1. 常温下,0.4mol•L-1一元酸HA与0.2mol•L-1NaOH溶液等体积混合后,所得溶液pH>7,溶液部分微粒组分及浓度如图所示.下列说法正确的( )
常温下,0.4mol•L-1一元酸HA与0.2mol•L-1NaOH溶液等体积混合后,所得溶液pH>7,溶液部分微粒组分及浓度如图所示.下列说法正确的( )
 常温下,0.4mol•L-1一元酸HA与0.2mol•L-1NaOH溶液等体积混合后,所得溶液pH>7,溶液部分微粒组分及浓度如图所示.下列说法正确的( )
常温下,0.4mol•L-1一元酸HA与0.2mol•L-1NaOH溶液等体积混合后,所得溶液pH>7,溶液部分微粒组分及浓度如图所示.下列说法正确的( )| A. | HA是弱酸 | |
| B. | 图中未表示出的微粒的浓度小于0.1mol/L | |
| C. | 该混合溶液中:c(HA)+c(X)═c(Na+) | |
| D. | 图中M表示HA,Y表示OH-,Z表示H+ |
18.用NaOH标准溶液滴定盐酸实验中,以下操作可能导致所测溶液浓度偏高的是( )
| A. | 滴定管用待装液润洗 | B. | 锥形瓶振荡时有少量液体溅出 | ||
| C. | 滴定结束后滴定管末端出现气泡 | D. | 锥形瓶用待测液润洗 |
20.以石墨为电极,电解足量KI溶液(并中含有少量酚酞和淀粉).下列说法正确的是( )
| A. | 阳极附近溶液呈无色 | B. | 溶液的pH变大 | ||
| C. | 阳极逸出气体 | D. | 阴极附近溶液呈蓝色 |