题目内容
 Ⅰ、(将2mol SO2和1mol O2气体在1L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2 (g) 2SO3 (g).若经过2s后测得SO3的浓度为0.6mol/L.试计算:(1)O2的化学反应速率V(O2)=
Ⅰ、(将2mol SO2和1mol O2气体在1L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2 (g) 2SO3 (g).若经过2s后测得SO3的浓度为0.6mol/L.试计算:(1)O2的化学反应速率V(O2)=Ⅱ、某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
(1)X的转化率是
(2)由图中所给数据进行分析,该反应的化学方程式为
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=
(4)当反应进行到第
考点:物质的量或浓度随时间的变化曲线,化学平衡的计算
专题:化学平衡专题
分析:Ⅰ、利用三段式计算各组成的浓度变化量、2s时各组成的浓度,若经过2s后测得SO3的浓度为0.6mol/L,物质的量=0.6mol/L×1L=0.6mol;
2SO2(g)+O2(g)?2SO3 (g)
起始量(mol) 2 1 0
变化量(mol) 0.6 0.3 0.6
2s时的量(mol) 1.4 0.7 0.6
根据v=
计算v(O2),根据c=
计算浓度;
Ⅱ、(1)根据平衡时用去的X的物质的量与起始的X的物质的量之比求得转化率;
(2)根据曲线的变化趋势判断反应物和生成物,根据物质的量变化之比等于化学计量数之比书写方程式;
(3)根据v=v=
计算反应速率;
(4)根据曲线的变化特点判断达到平衡的时间;
2SO2(g)+O2(g)?2SO3 (g)
起始量(mol) 2 1 0
变化量(mol) 0.6 0.3 0.6
2s时的量(mol) 1.4 0.7 0.6
根据v=
| △c |
| △t |
| n |
| V |
Ⅱ、(1)根据平衡时用去的X的物质的量与起始的X的物质的量之比求得转化率;
(2)根据曲线的变化趋势判断反应物和生成物,根据物质的量变化之比等于化学计量数之比书写方程式;
(3)根据v=v=
| △c |
| △t |
(4)根据曲线的变化特点判断达到平衡的时间;
解答:
解:Ⅰ、利用三段式计算各组成的浓度变化量、2s时各组成的浓度,若经过2s后测得SO3的浓度为0.6mol/L,物质的量=0.6mol/L×1L=0.6mol;
2SO2(g)+O2(g)?2SO3 (g)
起始量(mol) 2 1 0
变化量(mol) 0.6 0.3 0.6
2s量(mol) 1.4 0.7 0.6
O2的化学反应速率V(O2)=
=0.15mol/(L.s),
2s时的O2浓度=
=0.7mol/L;
故答案为:0.15mol/(L.s),0.7mol/L;
Ⅱ、(1)根据图象可知,平衡时用去的X的物质的量为0.3mol,起始的X的物质的量为1.0mol,故转化率为:
×100%=30%,故答案为:30%;
(2)从曲线的变化趋势可以看出,从反应开始到达到平衡,X、Y的物质的量减少,应为反应物,Z的物质的量增加,应为生成物,从反应开始到第2分钟反应到达平衡状态,X、Y消耗的物质的量分别为0.3 mol、0.1 mol,Z的生成的物质的量为0.2 mol,因此三者比例为3:1:2,
物质的量变化之比等于化学计量数之比,则化学方程式为3X+Y 2Z,
2Z,
故答案为:3X+Y 2Z;
2Z;
(3)v(Z)=
=
=0.05mol/(L?min),
故答案为:0.075mol/(L?min);
(4)从图象来看,第2分钟各物质的物质的量不再发生变化,因此第2分钟到达平衡状态,故答案为:2.
2SO2(g)+O2(g)?2SO3 (g)
起始量(mol) 2 1 0
变化量(mol) 0.6 0.3 0.6
2s量(mol) 1.4 0.7 0.6
O2的化学反应速率V(O2)=
| ||
| 2s |
2s时的O2浓度=
| 0.7mol |
| 1L |
故答案为:0.15mol/(L.s),0.7mol/L;
Ⅱ、(1)根据图象可知,平衡时用去的X的物质的量为0.3mol,起始的X的物质的量为1.0mol,故转化率为:
| 0.3mol |
| 1.0mol |
(2)从曲线的变化趋势可以看出,从反应开始到达到平衡,X、Y的物质的量减少,应为反应物,Z的物质的量增加,应为生成物,从反应开始到第2分钟反应到达平衡状态,X、Y消耗的物质的量分别为0.3 mol、0.1 mol,Z的生成的物质的量为0.2 mol,因此三者比例为3:1:2,
物质的量变化之比等于化学计量数之比,则化学方程式为3X+Y
 2Z,
2Z,故答案为:3X+Y
 2Z;
2Z;(3)v(Z)=
| △c |
| △t |
| ||
| 2min |
故答案为:0.075mol/(L?min);
(4)从图象来看,第2分钟各物质的物质的量不再发生变化,因此第2分钟到达平衡状态,故答案为:2.
点评:本题考查了物质的量随时间的变化曲线及化学反应三段式计算应用,主要是反应速率和浓度概念的计算,掌握基础是关键,题目难度不大,解题时应注意化学方程式的判断方法.

练习册系列答案
相关题目
有机物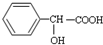 有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )
 有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )| A、6 种 |
| B、9 种 |
| C、15 种 |
| D、19 种 |
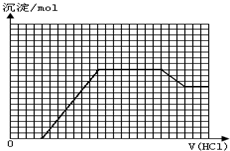 某无色溶液M可能含有离子OH-、HCO3-、CO32-、SO42-、SiO32-、AlO2-、NH4+、MnO4-、Cu2+、Mg2+、Na+、Fe3+中的若干种.取一定量的M溶液滴加盐酸,产生沉淀的物质的量与盐酸体积的关系如图所示.下列判断正确的是( )
某无色溶液M可能含有离子OH-、HCO3-、CO32-、SO42-、SiO32-、AlO2-、NH4+、MnO4-、Cu2+、Mg2+、Na+、Fe3+中的若干种.取一定量的M溶液滴加盐酸,产生沉淀的物质的量与盐酸体积的关系如图所示.下列判断正确的是( )| A、原溶液中可能含有NH4+、SO42- |
| B、最终溶液中最少含2种溶质 |
| C、原溶液中n(NaAlO2):n(Na2CO3)=1:1 |
| D、滴加盐酸初始阶段发生反应的离子方程式是:CO32-+H+=HCO3- |
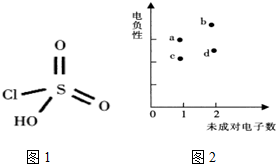 纯钛烤瓷牙是近几年才发展成熟的金属烤瓷技术,过氧硫酸被用于假牙的消毒.过氧硫酸可由氯磺酸通过反应I制得,氯磺酸结构如图1.
纯钛烤瓷牙是近几年才发展成熟的金属烤瓷技术,过氧硫酸被用于假牙的消毒.过氧硫酸可由氯磺酸通过反应I制得,氯磺酸结构如图1. (1)已知在一定条件下的反应4HCl+O2=2Cl2+2H2O中,有4mol HCl被氧化时,放出
(1)已知在一定条件下的反应4HCl+O2=2Cl2+2H2O中,有4mol HCl被氧化时,放出 托盘天平、容量瓶、滴定管、量筒是中学化学常见的计量仪器,熟知这些仪器的使用是定量研究化学的基础.
托盘天平、容量瓶、滴定管、量筒是中学化学常见的计量仪器,熟知这些仪器的使用是定量研究化学的基础.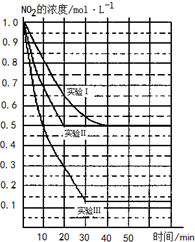 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为1.0mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题:
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为1.0mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题: