题目内容
碳和碳的化合物在生产生活实际中应用广泛.
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活.已知
①2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H1
②2CO(g)+O2(g)═2CO2(g)△H2
则反应CH4(g)+2O2(g)═CO2(g)+2H2O(l)的△H3= (用△H1和△H2表示).
(2)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L,则2NO2(g)?N2O4(g)的平衡常数K= (写出计算结果).
(3)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
回答下列问题:
①该反应为 反应(填“吸热”、“放热”).
②能使该反应速率增大的是 ;能使平衡向正反应方向移动的是 .
A.及时分离出CO气体 B.适当升高温度
C.增大CO2的浓度 D.选择高效催化剂.
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活.已知
①2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H1
②2CO(g)+O2(g)═2CO2(g)△H2
则反应CH4(g)+2O2(g)═CO2(g)+2H2O(l)的△H3=
(2)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L,则2NO2(g)?N2O4(g)的平衡常数K=
(3)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应为
②能使该反应速率增大的是
A.及时分离出CO气体 B.适当升高温度
C.增大CO2的浓度 D.选择高效催化剂.
考点:热化学方程式,化学平衡建立的过程,化学平衡的影响因素
专题:基本概念与基本理论
分析:(1)根据盖斯定律来计算化学反应的焓变;
(2)反应2NO2(g)?N2O4(g)的平衡常数表达式为:K=
,代入数据计算即可;
(3)①温度升高平衡常数增大,说明平衡向正反应方向移动;
②增大反应速率的因素有升温、加压、使用适当的催化剂、增大浓度等等;影响平衡移动的因素有温度、浓度和压强三因素,据勒夏特列原理解答.
(2)反应2NO2(g)?N2O4(g)的平衡常数表达式为:K=
| [N2O4] |
| [NO2]2 |
(3)①温度升高平衡常数增大,说明平衡向正反应方向移动;
②增大反应速率的因素有升温、加压、使用适当的催化剂、增大浓度等等;影响平衡移动的因素有温度、浓度和压强三因素,据勒夏特列原理解答.
解答:
解:(1)根据题意得CH4(g)+
O2(g)=CO(g)+2H2O(l)△H1=-607.3KJ/mol①,CO (g)+
O2(g)=CO2(g)△H2=-283kJ/mol②,
根据盖斯定律,①+②可得反应CH4(g)+2O2(g)=CO2(g)+2H2O (l) 的△H=-607.3KJ/mol+(-283kJ/mol)=-890.3KJ/mol,故答案为:-890.3KJ/mol;
(2)反应2NO2(g)?N2O4(g)的平衡常数表达式为:K=
=
=0.50(mol/L)-1,故答案为:0.50(mol/L)-1;
(3)①温度升高平衡常数增大,说明平衡向正反应方向移动,则正反应为吸热反应,故答案为:吸热;
②A、分离出CO,减慢反应速率,平衡正向移动;
B、反应速率加快,平衡正向移动;
C、增大CO2的浓度,反应速率加快,平衡正向移动;
D、使用适当催化剂,反应速率加快,平衡不移动;
故,能使该反应速率增大的是:BCD;能使平衡向正反应方向移动的是:ABC.
故答案为:BCD;ABC.
| 3 |
| 2 |
| 1 |
| 2 |
根据盖斯定律,①+②可得反应CH4(g)+2O2(g)=CO2(g)+2H2O (l) 的△H=-607.3KJ/mol+(-283kJ/mol)=-890.3KJ/mol,故答案为:-890.3KJ/mol;
(2)反应2NO2(g)?N2O4(g)的平衡常数表达式为:K=
| [N2O4] |
| [NO2]2 |
| 0.125mol/L |
| 0.50mol/L2 |
(3)①温度升高平衡常数增大,说明平衡向正反应方向移动,则正反应为吸热反应,故答案为:吸热;
②A、分离出CO,减慢反应速率,平衡正向移动;
B、反应速率加快,平衡正向移动;
C、增大CO2的浓度,反应速率加快,平衡正向移动;
D、使用适当催化剂,反应速率加快,平衡不移动;
故,能使该反应速率增大的是:BCD;能使平衡向正反应方向移动的是:ABC.
故答案为:BCD;ABC.
点评:本题考查盖斯定律、化学平衡常数及影响因素、影响化学反应速率的因素,难度中等,注意影响化学反应速率的因素主要有温度、浓度、压强、催化剂.

练习册系列答案
相关题目
关于CuSO4溶液和Fe(OH)3胶体描述正确的是( )
| A、两者颜色不一样 |
| B、两者外观上都不透明 |
| C、两者都能产生丁达尔现象 |
| D、两者不能产生丁达尔现象 |
可以判定某酸HA是弱电解质的事实是( )
| A、HA能与水以任意比互溶 |
| B、0.1mol?L-1HA溶液的pH约为3 |
| C、HA可与NaHCO3反应放出CO2 |
| D、HA溶液的导电能力很差 |
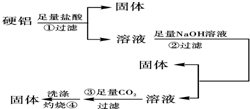 硬铝中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如图所示实验:
硬铝中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如图所示实验: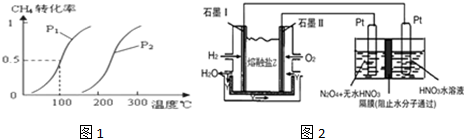
 ,其分子式为
,其分子式为