题目内容
下列反应中,二氧化硫既不是氧化剂又不是还原剂的是( )
| A、SO2+NO2→SO3+NO | ||
| B、SO2+2NaOH→H2O+Na2SO3 | ||
C、SO2+2Mg
| ||
| D、SO2+Br2+2H2O→H2SO4+2HBr |
考点:氧化还原反应
专题:氧化还原反应专题
分析:氧化还原反应的特征是元素化合价的升降,可从元素化合价的角度判断,反应中二氧化硫既不是氧化剂又不是还原剂,则S元素化合价不变,以此解答.
解答:
解:A.S元素化合价升高,被氧化,为还原剂,故A不选;
B.元素化合价没有发生变化,不是氧化还原反应,故B选;
C.S元素化合价降低,被还原,为氧化剂,故C不选;
D.S元素化合价升高,被氧化,为还原剂,故D不选.
故选B.
B.元素化合价没有发生变化,不是氧化还原反应,故B选;
C.S元素化合价降低,被还原,为氧化剂,故C不选;
D.S元素化合价升高,被氧化,为还原剂,故D不选.
故选B.
点评:本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,题目注重基础,难度较小,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的具有的性质.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
下列各装置中,不能构成原电池的是( )
A、 盐酸 |
B、 硫酸铜溶液 |
C、 稀硫酸 |
D、 稀硫酸 |
党的十七大报告指出:节约能源和保护环境是人类社会和谐发展的重要保证.下列做法中不符合这一要求的是( )
| A、推广使用沼气、太阳能、风能等新能源,减少煤、石油等化石燃料的使用 |
| B、研究采煤、采油新技术,提高产量以满足社会快速发展的需要 |
| C、垃圾分类回收,并对废旧电池回收处理 |
| D、提高汽车尾气的排放标准,减少机动车尾气污染 |
下列离子方程式书写正确的是( )
| A、少量的金属铜投入浓硝酸中Cu+4H++2NO3-=Cu2++NO2↑+2H2O |
| B、铝片投入稀盐酸中Al+6H+=Al3++3H2↑ |
| C、氢氧化钡溶液与稀硫酸混合Ba2++SO42-=BaSO4↓ |
| D、氢氧化铝与足量烧碱溶液混合Al(OH)3+OH-=AlO2-+2H2O |
下列关于化学反应速率和反应限度的说法正确的是( )
| A、不同形状的大理石与相同浓度的稀盐酸反应产生气体的速率:块状>粉末状 | |||
| B、不同浓度的硫酸溶解大小相同、形状相同铁片的速率:18 mol/L>3 mol/L | |||
| C、不同温度时,12%的过氧化氢溶液分解产生氧气的速率:60℃>30℃ | |||
D、2 mol SO2与足量O2在密闭容器中发生反应2SO2+O2
|

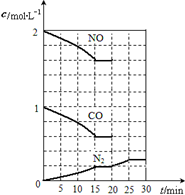 在铂-铑“三效”催化剂作用下,以下反应可以将汽车尾气中2种有
在铂-铑“三效”催化剂作用下,以下反应可以将汽车尾气中2种有