题目内容
13.100mL6mol/LH2SO4跟过量的锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量.可向反应物中加入适量的( )| A. | 碳酸钠(固体) | B. | 水 | C. | 硫酸钾溶液 | D. | 硫酸铵(固体) |
分析 为了减缓反应进行的速度,但又不影响生成氢气的总量,可降低氢离子浓度,但氢离子的总物质的量不变,以此解答该题.
解答 解:A.加入碳酸钠,消耗氢离子,反应速率降低,生成氢气总量减小,故A错误;
B.加入水,氢离子浓度减小,反应速率减小,但生成氢气的总量不变,故B正确;
C.硫酸钾溶液,硫酸钾不参与反应,但加入的水可使氢离子浓度减小,反应速率减小,但生成氢气的总量不变,故C正确;
D.加入硫酸铵(固体),由于硫酸铵水解呈酸性,氢离子浓度增大,反应速率增大,故D错误.
故选BC.
点评 本题考查化学反应速率的影响,侧重于基础知识的考查,为高考高频考点,难度不大,注意把握题目要求,易错点为D,注意铵根离子水解的性质.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
3.下列关于钠的说法中,不正确的是( )
| A. | 金属钠和氧气反应,条件不同,产物则不同 | |
| B. | 钠原子的最外层只有一个电子 | |
| C. | 钠的化学性质很活泼,少量的钠可以保存在煤油中 | |
| D. | 当钠与硫酸铜溶液反应时,有大量红色固体铜出现 |
4.某烃的结构简式为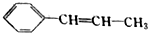 ,它可能具有的性质是( )
,它可能具有的性质是( )
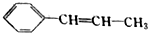 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水,也易溶于有机溶剂 | |
| B. | 既能使溴的四氯化碳溶液褪色,又能使酸性高锰酸钾溶液褪色 | |
| C. | 能发生聚合反应,其产物可表示为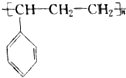 | |
| D. | 1mol该烃能与4molBr2发生加成反应 |
1.现有部分短周期元素的性质或原子结构如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的中子数是8.
(2)元素Y与R形成一种离子YR${\;}_{4}^{+}$,写出该微粒的电子式: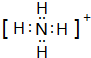 (用元素符号表示).它们还可以形成分子YR3,写出实验室制取该物质的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
(用元素符号表示).它们还可以形成分子YR3,写出实验室制取该物质的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是②.
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应.
| 元素编号 | 元素性质或原子结构 |
| R | 原子半径最小的元素 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y与R形成一种离子YR${\;}_{4}^{+}$,写出该微粒的电子式:
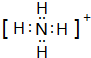 (用元素符号表示).它们还可以形成分子YR3,写出实验室制取该物质的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
(用元素符号表示).它们还可以形成分子YR3,写出实验室制取该物质的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是②.
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应.
8.常温下,0.1mol•L-1的下列溶液中,有关微粒的物质的量浓度关系正确的是( )
| A. | NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | (NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | NaHCO3溶液:c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
18.元素周期表和元素周期律可以指导人们进行规律性的推测和判断.下列说法不合理的是( )
| A. | 短周期元素正化合价数值和其族序数相同 | |
| B. | 人们可在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料 | |
| C. | 由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:F>Cl | |
| D. | 短周期元素形成的微粒X2-与 Y2+核外电子排布相同,离子半径:X2->Y2+ |
5.相同碳原子数的烷烃、烯烃、炔烃,在空气中完全燃烧生成二氧化碳和水,所需空气量的比较中正确的是
( )
( )
| A. | 烷烃最少 | B. | 烯烃最少 | C. | 炔烃最少 | D. | 三者一样多 |
2.下列说法正确的是( )
| A. | 乙酸与NaHCO3反应生成CO2气体,说明乙酸的酸性强于碳酸 | |
| B. | 乙烯使溴水褪色的反应方程式是:CH2=CH2+Br2→CH3CHBr2 | |
| C. | 乙烯和苯分子中都存在碳碳双键,都能发生加成反应 | |
| D. | 乙醇能发生氧化反应,乙酸不能发生氧化反应 |
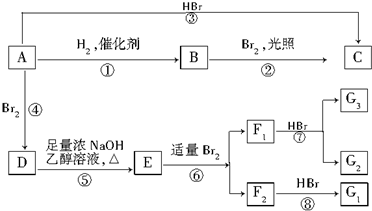
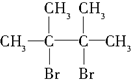 )(F1和F2互为同分异构体)(G1和G2互为同分异构体)
)(F1和F2互为同分异构体)(G1和G2互为同分异构体) .
.