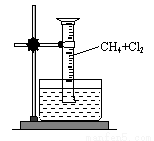
题目内容
高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如图:
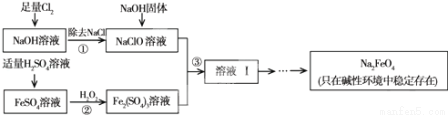
回答下列问题:
(1)经过步骤①后,加入NaOH固体的原因是 .
(2)步骤②反应的离子方程式是 .
(3)从溶液Ⅰ中分离出Na2FeO4后,还有副产品Na2SO4、NaCl,则步骤③中反应的离子方程式为 .
(4)将一定量的Na2FeO4投入到pH不同的污水中(污水中其余成分均相同),溶液中Na2FeO4浓度变化如图曲线Ⅰ、Ⅱ所示,试推测曲线Ⅰ比曲线Ⅱ对应的污水pH (填“高”或“低”).
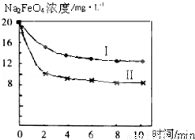
(5)通过计算得知Na2FeO4的消毒效率(以单位质量得到的电子数表示)比氯气的 (填“高”或“低”),用高铁酸钠代替氯气作净水消毒剂的优点是 (答出两点即可).
 阅读快车系列答案
阅读快车系列答案化学与社会、生活密切相关。对下列现象或事实的解释正确的是( )
选项 | 现象或事实 | 解释 |
A | SiO2用于制造光导纤维 | SiO2具有导电性 |
B | 用汽油洗去织物上的油污 | 汽油能与油污发生取代反应 |
C | 点燃铝热剂(Al和Fe2O3)焊接钢轨 | 铝置换出铁,并吸收能量使铁凝固 |
D | 泡沫灭火器是利用A | Al3+与HCO3-相互促进水解,生成阻燃性气体CO2,隔绝空气 |
某无色稀溶液X中,可能含有表所列离子中的某几种。现取该溶液适量,向 其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y体积(V)的关系如图所示,下列说法正确的是
其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y体积(V)的关系如图所示,下列说法正确的是
阴离子 | CO32﹣、SiO32﹣、AlO2﹣、Cl﹣ |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |

A.若Y是盐酸,则Oa段转化为沉淀的离子(表中,下同)只有AlO2﹣
B.若Y是盐酸,则溶液中可能含有的阳离子是Al3+
C.若Y是NaOH溶液,则bc段反应的离子方程式为
Al(OH)3+OH﹣═AlO2﹣+2H2O
D.若Y是NaOH溶液,则X溶液中只存在四种离子是:Al3+、Fe3+、NH4+、Cl﹣


 l2(SO4)3溶液与饱和NaHCO3溶液混合产生气体
l2(SO4)3溶液与饱和NaHCO3溶液混合产生气体 aL的氧气和氮气的混合物含有的分子数约为
aL的氧气和氮气的混合物含有的分子数约为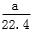 ×6.02×1023
×6.02×1023 2?SO4?3的酸性溶液中通入足量硫化氢Fe3++H2S=Fe2++S?+2H+
2?SO4?3的酸性溶液中通入足量硫化氢Fe3++H2S=Fe2++S?+2H+