题目内容
能正确表示下列反应的离子方程式为( )
| A、硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C、碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.硝酸具有氧化性,能氧化FeS,因此产物应该是硝酸铁、硫酸和一氧化氮;
B.漏掉氨根离子与氢氧根离子的反应;
C.碳酸钙溶于稀盐酸中,反应生成氯化钙和二氧化碳、水;
D.不符合反应的客观事实.
B.漏掉氨根离子与氢氧根离子的反应;
C.碳酸钙溶于稀盐酸中,反应生成氯化钙和二氧化碳、水;
D.不符合反应的客观事实.
解答:
解:A.硫化亚铁溶于稀硝酸中,离子方程式:FeS+4H++NO3-=Fe3++S↓+NO↑+2H2O,故A错误;
B.NH4HCO3溶于过量的NaOH溶液中,离子方程式:NH4++HCO3-+2OH-=CO32-+H2O+NH3?H2O,故B错误;
C.碳酸钙溶于稀盐酸中,离子方程式:CaCO3+2H+=Ca2++H2O+CO2↑,故C正确;
D.将铁粉加入稀硫酸中,离子方程式:Fe+2H+=Fe2++H2↑,故D错误;
故选:C.
B.NH4HCO3溶于过量的NaOH溶液中,离子方程式:NH4++HCO3-+2OH-=CO32-+H2O+NH3?H2O,故B错误;
C.碳酸钙溶于稀盐酸中,离子方程式:CaCO3+2H+=Ca2++H2O+CO2↑,故C正确;
D.将铁粉加入稀硫酸中,离子方程式:Fe+2H+=Fe2++H2↑,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意化学式的拆分、电荷的守恒,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图: | ||
B、H2O的电子式: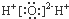 | ||
C、原子核内有10个中子的氧原子:
| ||
D、CO2的比例模型: |
物质的量相等的CO和CO2相比较,下列有关叙述中正确的是( )
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的C原子数目之比为1:1
⑤它们所含的电子数目之比为7:11.
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的C原子数目之比为1:1
⑤它们所含的电子数目之比为7:11.
| A、①和④ | B、②和③ |
| C、①②③④ | D、①②③④⑤ |
下列说法正确的是( )
| A、1mol任何气体所占体积都约为22.4L |
| B、1molH2O在标准状况下体积为22.4L |
| C、1mol气体体积为22.4L,则一定是标准状况 |
| D、气体摩尔体积不一定是22.4L/mol |
一定温度下,在容积为2L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示.则下列叙述不正确的是( )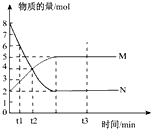

A、化学方程式中
| ||
| B、t2时N 的 v正=v逆. | ||
C、从t1到t2时刻 M的平均反应速率
| ||
| D、t3时混合气体的总物质的量不随时间的变化而变化 |
2013年宿迁市政府提出创建国家级卫生城市,提出了“人人参与,创建绿色家园”口号.下列说法不正确的是( )
| A、回收废旧电池 |
| B、加强控制燃放烟花爆竹 |
| C、停止使用含铅汽油 |
| D、将工厂烟囱加高,减少周围大气污染 |
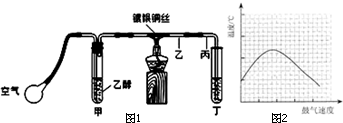 某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气.请填写下列空白:
某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气.请填写下列空白: