题目内容
4.下列排列顺序不正确的是( )| A. | 粒子半径:Al3+<Mg2+<F- | B. | 热稳定性:H2Te>H2Se>H2S>H2O | ||
| C. | 酸性:H2SiO3<H3PO4<H2SO4<HClO4 | D. | 金属性:Li<Na<K |
分析 A.三种离子的电子层数相同,离子的核电荷数越大,离子半径越小;
B.非金属性越强,对应氢化物的稳定性越强;
C.非金属性越强,最高价氧化物对应水合物的酸性越强;
D.同一主族中,原子序数越大,金属性越强.
解答 解:A.Al3+、Mg2+、F-都含有2个电子层,离子的核电荷数越大,离子半径越小,则离子半径大小为:Al3+<Mg2+<F-,故A正确;
B.同一主族中,原子序数越大,非金属性越弱,则非金属性:Te<Se<S<O;非金属性越强,氢化物稳定性越强,则热稳定性:H2Te<H2Se<H2S<H2O,故B错误;
C.非金属性:Si<P<S<Cl,则最高价氧化物对应水合物的酸性:H2SiO3<H3PO4<H2SO4<HClO4,故C正确;
D.Li、Na、K位于同一主族,原子序数逐渐增大,则金属性逐渐增强,则金属性:Li<Na<K,故D正确;
故选B.
点评 本题考查了原子结构与元素周期律的应用,题目难度不大,明确元素周期律内容为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
10.关于苯酚的说法中,错误的是( )
| A. | 纯净的苯酚是粉红色晶体 | |
| B. | 有特殊气味 | |
| C. | 常温时在水中溶解度不大,高于65℃时,能与水互溶 | |
| D. | 苯酚有毒,沾到皮肤上,可立即用酒精洗涤 |
11.“云蒸霞蔚”出自《世说新语•寓言》,表示霞光透过云层的绚丽灿烂.“云”从化学角度分析属于下列分散系中的( )
| A. | 溶液 | B. | 悬浊夜 | C. | 乳浊液 | D. | 胶体 |
12.下列现象中,因发生加成反应而产生的是( )
| A. | SO2使酸性高锰酸钾溶液褪色 | |
| B. | 将苯滴入溴水中,振荡后水层接近无色 | |
| C. | 乙烯使溴的四氯化碳溶液褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色消失 |
13. 利用如图装置进行实验,开始时,a、b 两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
利用如图装置进行实验,开始时,a、b 两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
 利用如图装置进行实验,开始时,a、b 两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
利用如图装置进行实验,开始时,a、b 两处液面相平,密封好,放置一段时间.下列说法不正确的是( )| A. | a 管发生吸氧腐蚀,b 管发生析氢腐蚀 | |
| B. | 一段时间后,a 管液面高于 b 管液面 | |
| C. | a 处溶液的 pH 增大,b 处溶液的 pH 减小 | |
| D. | a、b 两处具有相同的电极反应式:Fe-2e-═Fe2+ |
14.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 体心立方是金属最密堆积形式 | |
| B. | NaCl晶体的配位数为4 | |
| C. | 24g金刚石中含有C-C键的个数为4NA | |
| D. | 中和热测定时,用铜棒代替环形玻璃棒会导致△H偏低 |
 CH4
CH4 NaCl
NaCl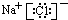
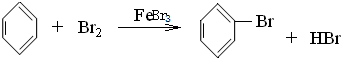
 .
.