题目内容
二氧化氮具有强氧化性,能氧化金属单质镁.某课题组探究镁和二氧化氮反应的产物.

(1)【提出假设】
他们根据氧化还原反应原理,提出如下假设一和二,请你完成假设三:
假设一:固体产物为Mg3N2;
假设二:固体产物为MgO;
假设三:固体产物为 .
(2)【理论分析】
类比镁在二氧化碳中燃烧反应,他们对镁与二氧化氮反应产物进行预测:写出镁在二氧化氮中反应的化学方程式: .
(3)【设计实验】
查阅资料知:2NO2+2NaOH═NaNO3+NaNO2+H2O他们设计实验装置(用于连接玻璃管的乳胶管均内衬锡箔)
①乳胶管内衬锡箔的目的是 .
②实验开始的操作步骤是 .
a.打开弹簧夹K b.当硬质玻璃管充满红棕色气体后,关闭弹簧夹K
c.点燃酒精灯 d.通入NO2
③干燥管作用是 ;B装置中试剂是 .
(4)【结果分析】
实验完成后,硬质玻璃管冷却至室温、称量,测得硬质玻璃管中剩余固体的质量为42.0g.将固体加入到水中产生有刺激气味的气体,该气体能使湿润的红色石蕊试纸变蓝色.C装置中收集的单质气体体积为2240mL(标准状况).写出玻璃管中发生反应的化学方程式: .

(1)【提出假设】
他们根据氧化还原反应原理,提出如下假设一和二,请你完成假设三:
假设一:固体产物为Mg3N2;
假设二:固体产物为MgO;
假设三:固体产物为
(2)【理论分析】
类比镁在二氧化碳中燃烧反应,他们对镁与二氧化氮反应产物进行预测:写出镁在二氧化氮中反应的化学方程式:
(3)【设计实验】
查阅资料知:2NO2+2NaOH═NaNO3+NaNO2+H2O他们设计实验装置(用于连接玻璃管的乳胶管均内衬锡箔)
①乳胶管内衬锡箔的目的是
②实验开始的操作步骤是
a.打开弹簧夹K b.当硬质玻璃管充满红棕色气体后,关闭弹簧夹K
c.点燃酒精灯 d.通入NO2
③干燥管作用是
(4)【结果分析】
实验完成后,硬质玻璃管冷却至室温、称量,测得硬质玻璃管中剩余固体的质量为42.0g.将固体加入到水中产生有刺激气味的气体,该气体能使湿润的红色石蕊试纸变蓝色.C装置中收集的单质气体体积为2240mL(标准状况).写出玻璃管中发生反应的化学方程式:
考点:性质实验方案的设计
专题:实验设计题,元素及其化合物
分析:(1)根据假设一:固体产物为Mg3N2;假设二:固体产物为MgO;得到假设三;
(2)二氧化碳与镁反应生成氧化镁和碳,据此类推,镁在二氧化氮中燃烧生成氧化镁、氮气;
(3)①二氧化氮能氧化腐蚀乳胶管;
②避免空气干扰实验,必须在加热之前排尽装置内空气,据此确定实验步骤;
③碱石灰以及氢氧化钠都可以和二氧化氮之间发生反应,据此确定装置的作用以及盛放的试剂;
(4)根据元素守恒以及质量关系进行计算各个物质的物质的量,物质的量之比等于方程式的系数之比,据此回答.
(2)二氧化碳与镁反应生成氧化镁和碳,据此类推,镁在二氧化氮中燃烧生成氧化镁、氮气;
(3)①二氧化氮能氧化腐蚀乳胶管;
②避免空气干扰实验,必须在加热之前排尽装置内空气,据此确定实验步骤;
③碱石灰以及氢氧化钠都可以和二氧化氮之间发生反应,据此确定装置的作用以及盛放的试剂;
(4)根据元素守恒以及质量关系进行计算各个物质的物质的量,物质的量之比等于方程式的系数之比,据此回答.
解答:
解:(1)根据假设一:固体产物为Mg3N2;假设二:固体产物为MgO;得到假设三:固体产物可能是氧化镁、氮化镁混合物,故答案为:MgO和Mg3N2;
(2)二氧化碳与镁反应生成氧化镁和碳,据此类推,得到:镁在二氧化氮中燃烧生成氧化镁、氮气,故答案为:4Mg+2NO2
4MgO+N2;
(3)①橡胶管含有碳碳双键,容易被强氧化剂二氧化氮氧化腐蚀,所以乳胶管内衬锡箔,故答案为:避免二氧化氮氧化(腐蚀)乳胶管;
②避免空气干扰实验,必须在加热之前排尽装置内空气,实验步骤为:打开弹簧夹K、通入二氧化氮、玻璃管内呈红棕色时关闭弹簧夹、加热玻璃管,故答案为:adbc;
③碱石灰以及氢氧化钠都可以和二氧化氮之间发生反应,干燥管中碱石灰用于吸收二氧化氮、B中溶液中用于吸收未反应的二氧化氮,可以选择氢氧化钠溶液,C装置用于收集氮气,故答案为:吸收二氧化氮,避免污染环境;氢氧化钠溶液;
(4)设固体产物中氧化镁的物质的量为a,氮化镁的物质的量为b.
a+3b=1.1mol,a×40g/mol+b×100g/mol=42.0g,解得:a=0.80mol,b=0.1mol,n(N2)=
=0.1mol,所以MgO、Mg3N2、N2的物质的量之比=方程式的系数之比=8:1:1,由此根据原子守恒得出化学方程式为:11Mg+4NO2
Mg3N2+8MgO+N2,故答案为:11Mg+4NO2
Mg3N2+8MgO+N2.
(2)二氧化碳与镁反应生成氧化镁和碳,据此类推,得到:镁在二氧化氮中燃烧生成氧化镁、氮气,故答案为:4Mg+2NO2
| ||
(3)①橡胶管含有碳碳双键,容易被强氧化剂二氧化氮氧化腐蚀,所以乳胶管内衬锡箔,故答案为:避免二氧化氮氧化(腐蚀)乳胶管;
②避免空气干扰实验,必须在加热之前排尽装置内空气,实验步骤为:打开弹簧夹K、通入二氧化氮、玻璃管内呈红棕色时关闭弹簧夹、加热玻璃管,故答案为:adbc;
③碱石灰以及氢氧化钠都可以和二氧化氮之间发生反应,干燥管中碱石灰用于吸收二氧化氮、B中溶液中用于吸收未反应的二氧化氮,可以选择氢氧化钠溶液,C装置用于收集氮气,故答案为:吸收二氧化氮,避免污染环境;氢氧化钠溶液;
(4)设固体产物中氧化镁的物质的量为a,氮化镁的物质的量为b.
a+3b=1.1mol,a×40g/mol+b×100g/mol=42.0g,解得:a=0.80mol,b=0.1mol,n(N2)=
| 2.24L |
| 22.4L/mol |
| ||
| ||
点评:本题是一道物质性质的实验方案设计题,考查学生分析和解决问题的能力,难度大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
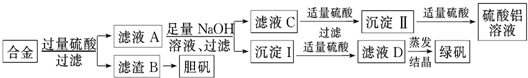
某溶液中可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+,进行如下实验:
(1)取该溶液100mL,加入过量NaOH溶液,加热,得到0.01 mol 气体,同时产生红褐色沉淀;过滤,将沉淀洗涤,灼烧,得到0.8 g固体;
(2)向(1)的滤液中通入足量CO2,过滤,得到0.01 mol沉淀;
(3)向(2)的滤液中加入足量用盐酸酸化的BaCl2溶液,得到2.33g沉淀,
由此可知原溶液中( )
(1)取该溶液100mL,加入过量NaOH溶液,加热,得到0.01 mol 气体,同时产生红褐色沉淀;过滤,将沉淀洗涤,灼烧,得到0.8 g固体;
(2)向(1)的滤液中通入足量CO2,过滤,得到0.01 mol沉淀;
(3)向(2)的滤液中加入足量用盐酸酸化的BaCl2溶液,得到2.33g沉淀,
由此可知原溶液中( )
| A、至少存在CO32-、Cl-中的一种 |
| B、Cl-一定存在,K+可能存在 |
| C、Cl-一定存在,且c(Cl-)≥0.6mol?L-1 |
| D、溶液中至少存在4种离子 |
按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物,下列说法错误的是( )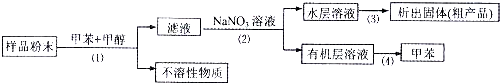

| A、步骤(1)需要用到过滤装置 |
| B、步骤(2)需要用到分液装置 |
| C、步骤(3)需要用到蒸发皿 |
| D、步骤(4)需要用到布氏漏斗 |
下列物质的转化在给定条件下能实现的是( )
| A、AlCl3(aq)\underrightarrowNH3NaAlO2(aq)\underrightarrowCO2Al(OH)3 | ||
B、MgCl2(熔融)\underrightarrow电解Mga
| ||
| C、FeS2\underrightarrow燃烧SO3\underrightarrowH2OH2SO4 | ||
D、NaCl(aq)\underrightarrow电解Na
|
甲、乙、丙、丁甲种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系、:甲
乙
丙.下列有关物质的推断不正确的是( )
| 丁 |
| 丁 |
| 甲 |
| A、若甲为焦炭,则丁可能是O2 |
| B、若甲为SO2,则丁可能是氨水 |
| C、若甲为NaAlO2溶液,则丁可能是盐酸 |
| D、若甲为CuCl2,则丁可能是氨水. |
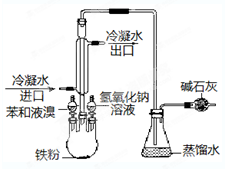 如图是实验室制取溴苯的装置图:
如图是实验室制取溴苯的装置图: