题目内容
下列反应中,可用离子方程式M+2H+=M2++H2↑表示的是(M表示金属单质)( )
①钠和稀H2SO4反应 ②锌和稀H2SO4反应 ③镁和醋酸反应 ④铁和浓HCl反应 ⑤铝和稀HCl反应.
①钠和稀H2SO4反应 ②锌和稀H2SO4反应 ③镁和醋酸反应 ④铁和浓HCl反应 ⑤铝和稀HCl反应.
| A、①④ | B、①②⑤ | C、②④ | D、③④ |
考点:离子方程式的书写
专题:离子反应专题
分析:离子方程式M+2H+=M2++H2↑中,金属M与非氧化性强酸反应生成的离子必须为+2价离子,即必须满足两个条件:①酸必须为非氧化性强电解质,如盐酸、稀硫酸,不能为硝酸;②金属与氢离子反应后必须生成+2价阳离子,如铁、锌、镁等,不能为钠、铝等金属,据此进行解答.
解答:
解:①钠和稀H2SO4反应:钠为+1价金属,反应生成Na+,离子方程式为2Na+2H+=2Na++H2↑,不能用M+2H+=M2++H2↑表示,故①错误;
②锌和稀H2SO4反应:锌为2价金属,稀硫酸为非氧化性强酸,锌与稀硫酸反应的离子方程式为:Zn+2H+=Zn2++H2↑,可以用M+2H+=M2++H2↑表示,故②正确;
③镁和醋酸反应:醋酸为弱酸,离子方程式中醋酸不能拆开,应该保留分子式CH3COOH,反应的离子方程式为:Mg+2CH3COOH=Mg2++2CH3COO-+H2↑表示,不能用M+2H+=M2++H2↑表示,故③错误;
④铁和浓HCl反应:铁与盐酸反应生成氯化亚铁和氢气,离子方程式为:Fe+2H+=Fe2++H2↑,可以用M+2H+=M2++H2↑表示,故④正确;
⑤铝和稀HCl反应:Al为3价金属,铝与稀盐酸反应达到离子方程式为:2Al+6H+=2Al3++3H2↑,不能用M+2H+=M2++H2↑表示,故⑤错误;
根据以上分析可知,可用离子方程式M+2H+=M2++H2↑表示的是②④,
故选C.
②锌和稀H2SO4反应:锌为2价金属,稀硫酸为非氧化性强酸,锌与稀硫酸反应的离子方程式为:Zn+2H+=Zn2++H2↑,可以用M+2H+=M2++H2↑表示,故②正确;
③镁和醋酸反应:醋酸为弱酸,离子方程式中醋酸不能拆开,应该保留分子式CH3COOH,反应的离子方程式为:Mg+2CH3COOH=Mg2++2CH3COO-+H2↑表示,不能用M+2H+=M2++H2↑表示,故③错误;
④铁和浓HCl反应:铁与盐酸反应生成氯化亚铁和氢气,离子方程式为:Fe+2H+=Fe2++H2↑,可以用M+2H+=M2++H2↑表示,故④正确;
⑤铝和稀HCl反应:Al为3价金属,铝与稀盐酸反应达到离子方程式为:2Al+6H+=2Al3++3H2↑,不能用M+2H+=M2++H2↑表示,故⑤错误;
根据以上分析可知,可用离子方程式M+2H+=M2++H2↑表示的是②④,
故选C.
点评:本题考查了离子方程式的正误判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
铜-锌原电池如图所示,下列叙述正确的是( )
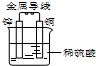

| A、氢离子在负极得电子 |
| B、锌为负极,发生氧化反应 |
| C、铜片上无气泡产生 |
| D、电子从铜片经金属导线流向锌片 |
日本福岛核事故释放的人工放射性碘
I,半衰期为8.3天,该同位素原子核内的中子数与核外电子数之差是( )
131 53 |
| A、25 | B、78 | C、53 | D、131 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温下,16gCH4含有10NA个电子 |
| B、标准状况下,22.4L苯含有NA个苯分子 |
| C、标准状况下,6.72LNO2与水充分反应转移的电子数目为0.1NA |
| D、0.1mol.L-1CH3COOH溶液中含有0.1NA个CH3COO- |
下列生产工艺能体现“绿色化学”或节能环保思想的是( )
| A、工业制氢气:用天然气发电再电解水制得 |
| B、工业制硫酸:提高尾气排放的烟窗高度 |
| C、工业制胆矾:使用向稀硫酸中吹空气并加热溶解铜 |
| D、降低PM2.5:用油改煤技术,推广优质煤的使用范围 |
下列各类烃中,碳氢两元素的质量比为定值的是( )
| A、烷烃 | B、环烷烃 |
| C、烯烃 | D、苯的同系物 |