题目内容
当1g氨气完全分解为氮气、氢气时,吸收2.72kJ的热量,则下列热化学方程式正确的是( )①N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ/mol
②N2(g)+3H2(g)═2NH3(g)△H=-46.2kJ/mol
③NH3(g)═
 N2(g)+
N2(g)+ H2(g)△H=+46.2kJ/mol
H2(g)△H=+46.2kJ/mol④2NH3(g)═N2(g)+3H2(g)△H=-92.4kJ/mol.
A.①②
B.①③
C.①②③
D.全部
【答案】分析:n(NH3)=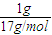 =
=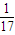 mol,则分解1molNH3吸收17×2.72kJ=46.24kJ能量,生成1molNH3放出46.24kJ能量,热量多少与各物质的化学计量数或物质的量有关.
mol,则分解1molNH3吸收17×2.72kJ=46.24kJ能量,生成1molNH3放出46.24kJ能量,热量多少与各物质的化学计量数或物质的量有关.
解答:解:n(NH3)=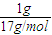 =
=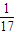 mol,则分解1molNH3吸收17×2.72kJ=46.24kJ能量,生成1molNH3放出46.24kJ能量,则
mol,则分解1molNH3吸收17×2.72kJ=46.24kJ能量,生成1molNH3放出46.24kJ能量,则
生成2molNH3放出2×46.24kJ≈92.4kJ,故①正确,②错误;
③分解1molNH3吸收17×2.72kJ=46.24kJ能量,故③正确;
④分解2molNH3吸收92.4kJ能量,而不是放出,故④错误,
故选B.
点评:本题考查热化学方程式,题目难度不大,注意书写热化学方程式时,要标明物质的状态,其热量多少与各物质的化学计量数或物质的量有关,△H>0表明是吸收热量,△H<0表明是放出热量.
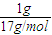 =
=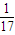 mol,则分解1molNH3吸收17×2.72kJ=46.24kJ能量,生成1molNH3放出46.24kJ能量,热量多少与各物质的化学计量数或物质的量有关.
mol,则分解1molNH3吸收17×2.72kJ=46.24kJ能量,生成1molNH3放出46.24kJ能量,热量多少与各物质的化学计量数或物质的量有关.解答:解:n(NH3)=
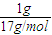 =
=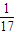 mol,则分解1molNH3吸收17×2.72kJ=46.24kJ能量,生成1molNH3放出46.24kJ能量,则
mol,则分解1molNH3吸收17×2.72kJ=46.24kJ能量,生成1molNH3放出46.24kJ能量,则生成2molNH3放出2×46.24kJ≈92.4kJ,故①正确,②错误;
③分解1molNH3吸收17×2.72kJ=46.24kJ能量,故③正确;
④分解2molNH3吸收92.4kJ能量,而不是放出,故④错误,
故选B.
点评:本题考查热化学方程式,题目难度不大,注意书写热化学方程式时,要标明物质的状态,其热量多少与各物质的化学计量数或物质的量有关,△H>0表明是吸收热量,△H<0表明是放出热量.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
 N2(g)+
N2(g)+ H2(g)△H=+46.2kJ/mol
H2(g)△H=+46.2kJ/mol