题目内容
A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素.已知:
①热稳定性:HmD>HmC;
②Cm-、E(m-1)-具有相同的电子层结构;
③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;
④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应.依据上述信息用相应的化学用语回答下列问题:
(1)HmD的电子式: .
(2)Cm-和E(m-1)-的还原性强弱为 > ,能证明其还原性强弱的化学方程式为 (3)用电子式表示A和E形成化合物的过程: .
(4)写出B的最高价氧化物对应的水化物和A的最高价氧化物对应的水化物反应的化学方程式 .
①热稳定性:HmD>HmC;
②Cm-、E(m-1)-具有相同的电子层结构;
③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;
④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应.依据上述信息用相应的化学用语回答下列问题:
(1)HmD的电子式:
(2)Cm-和E(m-1)-的还原性强弱为
(4)写出B的最高价氧化物对应的水化物和A的最高价氧化物对应的水化物反应的化学方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:根据题意,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应,所以B为Al元素,又因为A、B所形成的单核离子具有相同的电子层结构,所以A为Na元素;根据B与E在同一周期,在该周期中,E的原子半径最小,所以E为Cl元素;根据Cm-、E(m-1)-具有相同的电子层结构,所以C为S元素;根据热稳定性:HmD>HmC,所以D为O元素,以此解答该题.
解答:
解:依据分析可知:A为钠,B为铝,C为硫,D为氧,E为氯,
(1)HmD为H2O,为共价化合物,电子式为 ,故答案为:
,故答案为: ;
;
(2)由于非金属性Cl>S,单质的氧化性Cl2>S,单质的氧化性越强,对应阴离子的还原性越弱,则有还原性:S2->Cl-,可通过反应Cl2+S2-=2Cl-+S↓证明,故答案为:S2-;Cl-;Cl2+S2-=2Cl-+S↓;
(3)Na和Cl形成化合物为氯化钠,属于离子化合物,其形成过程为: ,故答案为:
,故答案为: ;
;
(4)Al(OH)3具有两性,与NaOH反应生成NaAlO2和H2O,反应的离子方程式为Al(OH)3+NaOH=NaAlO2+2H2O,故答案为:Al(OH)3+NaOH=NaAlO2+2H2O.
(1)HmD为H2O,为共价化合物,电子式为
 ,故答案为:
,故答案为: ;
;(2)由于非金属性Cl>S,单质的氧化性Cl2>S,单质的氧化性越强,对应阴离子的还原性越弱,则有还原性:S2->Cl-,可通过反应Cl2+S2-=2Cl-+S↓证明,故答案为:S2-;Cl-;Cl2+S2-=2Cl-+S↓;
(3)Na和Cl形成化合物为氯化钠,属于离子化合物,其形成过程为:
 ,故答案为:
,故答案为: ;
;(4)Al(OH)3具有两性,与NaOH反应生成NaAlO2和H2O,反应的离子方程式为Al(OH)3+NaOH=NaAlO2+2H2O,故答案为:Al(OH)3+NaOH=NaAlO2+2H2O.
点评:本题考查位置结构性质的关系及应用,题目难度不大,正确推断元素的种类为解答该题的关键.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
下列溶液中的c(Cl-)与50mL 1mol?L-1AlCl3溶液中的c(Cl-)不相等的是( )
| A、150mL 1mol?L-1氯化钠溶液 |
| B、75mL 1.5 mol?L-1氯化钙溶液 |
| C、150mL 3 mol?L-1氯化钾溶液 |
| D、75mL 1 mol?L-1氯化铁溶液 |
NA为阿伏加德罗常数,下列描述正确的是( )
| A、含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| B、1 L l mol/L的盐酸溶液含溶质HCl分子数为NA |
| C、标准状况下,11.2 L四氯化碳所含分子数为0.5NA |
| D、常温常压下,5.6g铁与过量的盐酸反应转移电子总数为0.2NA |
“绿色商品”是对环境无污染的商品,下列商品不能称为“绿色商品”的是( )
| A、无铅汽油 | B、无磷洗涤剂 |
| C、无氟冰箱 | D、无碘食盐 |
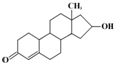 “诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图下列关于“诺龙”的说法中不正确的是( )
“诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图下列关于“诺龙”的说法中不正确的是( )| A、分子式是C18H26O2 |
| B、能在NaOH醇溶液中发生消去反应 |
| C、既能发生加成反应,也能发生酯化反应 |
| D、既能发生氧化反应,也能发生还原反应 |
某温度下,在一个1L的密闭容器中,加人4molA和2molB进行如下反应:3A(g)+2B(g)?4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
A、该反应的化学平衡常数表达式是K=
| ||
| B、此时,B的平衡转化率是35% | ||
| C、增大该体系的压强,平衡向右移动,化学平衡常数增大 | ||
| D、增加C,B的平衡转化率不变 |
