题目内容
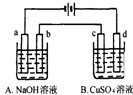 按如图装置进行电解(均是惰性电极),已知A烧杯中装有500mL20%的NaOH溶液,B烧杯中装有500mL pH为6的1mol?L-1CuSO4溶液.通电一段时间后,在b电极上收集到28mL气体(标准状况),则B烧杯中溶液pH变为(溶液体积变化忽略不计)( )
按如图装置进行电解(均是惰性电极),已知A烧杯中装有500mL20%的NaOH溶液,B烧杯中装有500mL pH为6的1mol?L-1CuSO4溶液.通电一段时间后,在b电极上收集到28mL气体(标准状况),则B烧杯中溶液pH变为(溶液体积变化忽略不计)( )| A、4 | B、3 | C、2 | D、1 |
考点:原电池和电解池的工作原理,电解原理
专题:电化学专题
分析:a、c是阴极,b、d是阳极,b、d极上的电极反应为:4OH--4e-=2H2O+O2↑,a极方程式为2H++2e-═H2↑,c极上的电极反应为:Cu2++2e-=Cu,结合电极方程式计算.
解答:
解:b极上的电极反应为:4OH--4e-=2H2O+O2↑,n(O2)=
=0.00125mol,
则转移电子的物质的量为0.00125mol×4=0.005mol,
B电解池发生2CuSO4+2H2O
2Cu+O2↑+2H2SO4,可知生成0.005molH+,
c(H+)=
=0.01mol/L,
则pH=2,
故选C.
| 0.028L |
| 22.4L/mol |
则转移电子的物质的量为0.00125mol×4=0.005mol,
B电解池发生2CuSO4+2H2O
| ||
c(H+)=
| 0.005mol |
| 0.5L |
则pH=2,
故选C.
点评:本题考查电解原理,侧重于学生的分析能力和计算能力的考查,为高考高频考点,难度中等,注意把握离子的放电顺序,为解答该题的关键.

练习册系列答案
相关题目
下列说法,正确的是( )
| A、第三周期非金属元素对应含氧酸的酸性从左到右都是依次增强 |
| B、HF、HCI、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| C、离子化合物中阴、阳离子间存在静电吸引力 |
| D、短周期元素形成离子后,最外层电子都达到8电子稳定结构 |
下列说法正确的是( )
| A、1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1 mol?L-1 |
| B、从1L2 mol?L-1的硫酸溶液中取出0.5L,该溶液的浓度为1 mol?L-1 |
| C、配制500mL0.5 mol?L-1的硫酸铜溶液,需要62.5g胆矾 |
| D、中和100mL1 mol?L-1的硫酸溶液,需要NaOH 4g |
分离水和汽油的混合物,可选用的分离方法为( )
| A、过滤法 | B、加热分解法 |
| C、蒸馏法 | D、分液法 |
下列说法或表示方法正确的是( )
| A、反应物总能量低于生成物总能量时,该反应不能发生 |
| B、氢气燃烧热的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
| C、甲烷是清洁、无污染的化石燃料 |
| D、氢气是热值高、无污染的燃料 |
科学家发现海洋是一个名副其实的“聚宝盆”,一些国家觊觎我国南海海域的丰富资源,导致近年来南海争端不断.下列对海洋资源开发利用的说法不正确的是( )
| A、海底如“土豆”般的金属结核矿含有铁、锰、钴等多种元素,可用铝热法冶炼并分离得到各种金属单质 |
| B、海水淡化工厂可与化工生产结合,如淡化后的浓海水,可用于提溴、镁、钠等 |
| C、海水中的金、铀等元素储量高、浓度低,提炼时,须先富集 |
| D、海水提镁过程中,所需的石灰乳,可用贝壳煅烧后加水得到,体现了就地取材、降低成本的生产理念 |
下列条件下,两瓶气体所含原子数一定相等的是( )
| A、同压强、同温度的N2和CO |
| B、同温度、同体积的H2和N2 |
| C、同体积、同密度的C2H4和C3H6 |
| D、同压强、同体积的N2O和CO2 |