题目内容
18.某元素R原子核外共有3个电子层,它的M层上的轨道排布式局部为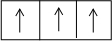 :下列对这种元素的分析中正确的( )
:下列对这种元素的分析中正确的( )| A. | 最外层电子数为3 | |
| B. | 最高价氧化物对应水化物的分子式可能是H3RO4 | |
| C. | 最高价为+3价 | |
| D. | 此元素可能是24号元素铬(Cr)或25号元素锰(Mn) |
分析 某元素R原子核外共有3个电子层,它的M层上的轨道排布式局部为 ,该原子核外电子排布式为1s22s22p63s23p3,为P元素,P的最外层有5个电子;最高正价为+5价,最高价氧化物对应水化物的分子式可能是H3PO4;最高正价等于主族序数,为+5价.
,该原子核外电子排布式为1s22s22p63s23p3,为P元素,P的最外层有5个电子;最高正价为+5价,最高价氧化物对应水化物的分子式可能是H3PO4;最高正价等于主族序数,为+5价.
解答 解:某元素R原子核外共有3个电子层,它的M层上的轨道排布式局部为 ,该原子核外电子排布式为1s22s22p63s23p3,为P元素,
,该原子核外电子排布式为1s22s22p63s23p3,为P元素,
A.P的最外层有5个电子,故A错误;
B.最高正价为+5价,最高价氧化物对应水化物的分子式可能是H3PO4,故B正确;
C.最高正价等于主族序数,为+5价,故C错误;
D.根据上述分析,该元素为P,故D错误;
故选B.
点评 本题考查原子核外电子排布,为高频考点,明确原子构造原理及原子核外电子排布规律是解本题关键,题目难度不大.

练习册系列答案
相关题目
9.下列有关(NH4)Al(SO4)2溶液的叙述正确的是( )
| A. | 能大量存在:Na+、C6H5O-、Cl-、Br- | |
| B. | 同温下通入少量的氨气:NH4+的水解能力增强,Kw增大,有白色沉淀产生 | |
| C. | 加入Ba(OH)2溶液生成沉淀质量最多的离子方程式:NH4++Al3++2Ba2++5OH-+2SO42-=2BaSO4↓+AlO2-+NH3•H2O+2H2O | |
| D. | 其浓溶液可与NaHCO3溶液混合制成灭火器 |
13.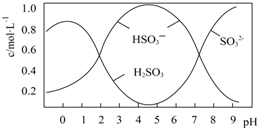 葡萄酒常用Na2S2O5做抗氧化剂,25℃时,将0.5molNa2S2O5溶于水配成1L溶液,该溶液pH=4.5,溶液中部分微粒不正确的是( )
葡萄酒常用Na2S2O5做抗氧化剂,25℃时,将0.5molNa2S2O5溶于水配成1L溶液,该溶液pH=4.5,溶液中部分微粒不正确的是( )
 葡萄酒常用Na2S2O5做抗氧化剂,25℃时,将0.5molNa2S2O5溶于水配成1L溶液,该溶液pH=4.5,溶液中部分微粒不正确的是( )
葡萄酒常用Na2S2O5做抗氧化剂,25℃时,将0.5molNa2S2O5溶于水配成1L溶液,该溶液pH=4.5,溶液中部分微粒不正确的是( )| A. | Na2S2O5溶于水的化学方程式:Na2S2O5+H2O=2NaHSO3 | |
| B. | 由图形可知,25℃时,HSO3-的水解平衡常数约为10-12 | |
| C. | 当溶液pH小于0.5后,图中曲线变化的原因可能是H2SO3被部分氧化 | |
| D. | 向溶液中加入碱性物质使溶液pH升高的过程中,一定存在如下关系:c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-) |
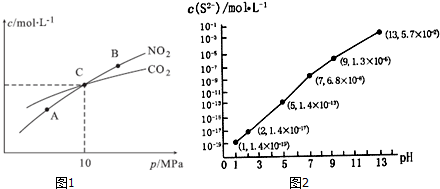
6.已知300℃、70MPa下由二氧化碳和氢气合成乙醇的反应成为现实:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H<0.在温度为T℃,容积不变的V L密闭容器中,将3mol H2和1mol CO2混合,达到平衡时乙醇气体的体积分数为a,下列有关说法正确的是( )
| A. | 升高温度,该反应的平衡常数将增大 | |
| B. | 从平衡混合气中分离出水蒸气可提高CO2和H2的利用率 | |
| C. | 再向该容器中充入2 mol H2和1 mol CO2,达到平衡时,H2的转化率将小于CO2 | |
| D. | T℃,在起始体积为V L的密闭容器(容积可变,恒压)中将3 mol H2和1 mol CO2混合,达到平衡时乙醇体积分数大于a |
3.化学与资源、环境、生活关系密切,下列说法正确的是( )
| A. | 二氧化硫有毒,严禁将其添加到任何食品和饮料中 | |
| B. | “氟化物防治龋齿”是应用了沉淀转化的原理,产生更能抵抗酸侵蚀的物质 | |
| C. | 使用增塑剂-邻苯二甲酸酯可使聚氯乙烯由弹性塑胶变为硬塑胶 | |
| D. | 面粉生产中禁止添加的过氧化钙(CaO2)中阴阳离子的个数比为1:2 |
4.下列说法不正确的是( )
| A. | 实验探究Zn-Cu及稀硫酸原电池工作原理,在稀硫酸溶液中加少量重铬酸钾因其有去极化作用可延长灯泡发亮时间,重铬酸钾也可用 KMnO4、MnO2等强氧化性物质代替 | |
| B. | 一些有机溶剂(如乙醚、苯、丙酮等)沸点低且极易被引燃,加热时最好用水浴加热 | |
| C. | 在醋酸钠溶液中滴人酚酞试液,加热后红色加深,可证明盐类水解是吸热反应 | |
| D. | 可使用溴水鉴别植物油和汽油 |

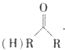 $\stackrel{HCN}{→}$
$\stackrel{HCN}{→}$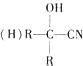 $→_{H+}^{H_{2}O}$
$→_{H+}^{H_{2}O}$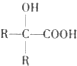
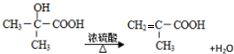
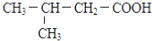 B.
B.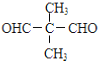 C.
C.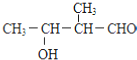 D.
D.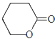
 .
. )可以生物降解,实现在自然界中的循环,是理想的绿色高分 子材料.请以乙醛为有机原料,设计聚乳酸的合成路线.(无机试剂任选,合成路线参照“已 知”中的书写形式)
)可以生物降解,实现在自然界中的循环,是理想的绿色高分 子材料.请以乙醛为有机原料,设计聚乳酸的合成路线.(无机试剂任选,合成路线参照“已 知”中的书写形式) .
.