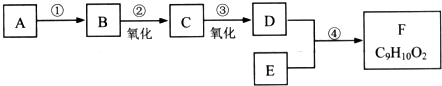
题目内容
有A、B、C、D、E五种短周期元素,其元素特征信息如表:
回答下列问题:
(1)写出下列元素的名称:B、 ,C、 ,D、 ,E、 ;
(2)写出A、B、C形成的化合物M的化学式 ;
(3)实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为 ;
(4)D单质与M的水溶液反应的离子方程式: .
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质,在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为倍受青睐的清洁燃料. |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一,工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障. |
| C | 其阳离子与B的阴离子有相同的电子层结构, 且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(1)写出下列元素的名称:B、
(2)写出A、B、C形成的化合物M的化学式
(3)实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为
(4)D单质与M的水溶液反应的离子方程式:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A其单质是密度最小的物质,在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为倍受青睐的清洁燃料,故A是氢;
B的阴离子带两个单位负电荷,单质是空气的主要成分之一,工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障,故B是氧;
C的阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物,故C是钠;
D的氢氧化物和氧化物都有两性,与C同周期,故D是铝;
E与C同周期,原子半径在该周期最小,故E是氯,据此解答各小题即可.
B的阴离子带两个单位负电荷,单质是空气的主要成分之一,工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障,故B是氧;
C的阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物,故C是钠;
D的氢氧化物和氧化物都有两性,与C同周期,故D是铝;
E与C同周期,原子半径在该周期最小,故E是氯,据此解答各小题即可.
解答:
解:依据分析可知:A为氢,B为氧,C为钠,D为铝,E为氯,
(1)B、氧,C、钠,D、铝,E、氯,故答案为:氧、钠、铝、氯;
(2)H、O、Na形成的化合物M为氢氧化钠,其化学式NaOH,故答案为:NaOH;
(3)DE3为AlCl3,已知其在熔化状态下不导电,故其是共价化合物,含有共价键,故答案为:共价键;
(4)D为铝,与氢氧化钠反应生成氢气和偏铝酸钠,离子反应方程式为:Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:Al+2OH-+2H2O=2AlO2-+3H2↑.
(1)B、氧,C、钠,D、铝,E、氯,故答案为:氧、钠、铝、氯;
(2)H、O、Na形成的化合物M为氢氧化钠,其化学式NaOH,故答案为:NaOH;
(3)DE3为AlCl3,已知其在熔化状态下不导电,故其是共价化合物,含有共价键,故答案为:共价键;
(4)D为铝,与氢氧化钠反应生成氢气和偏铝酸钠,离子反应方程式为:Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:Al+2OH-+2H2O=2AlO2-+3H2↑.
点评:本题主要考查的是元素的推断以及元素化合物的性质,推断出各种元素是关键,属于常考题.

练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
关于化学反应的△H的理解正确的是( )
| A、△H>0的反应是吸热反应 |
| B、△H=ΣH(反应物)-ΣH(生成物) |
| C、所有化学反应的△H都可以通过实验测出 |
| D、△H=反应中化学键形成时吸收的总能量-反应中化学键断裂时放出的总能量 |
下列叙述中,正确的是( )
| A、1 mol 乙烯分子中含有共价键的数目为7NA |
| B、1 mol甲基(-CH3)中含有电子的数目为10NA |
| C、标准状况下,1L戊烷在空气中完全燃烧生成5/22.4 L的CO2 |
| D、14 g乙烯和丙烯的混合物中含有碳原子的数目为NA |
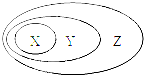 用图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用图表示的一些物质或概念之间的从属或包含关系中,错误的是( )