题目内容
下列相关反应的离子方程式书写错误的是( )
| A、Cl2与FeSO4溶液反应:Cl2+2Fe2+=2Cl-+2Fe3+ |
| B、等体积、等物质的量浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、用稀硫酸酸化的KMnO4溶液与少量H2O2反应:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
| D、SO2通入NaClO溶液中:SO2+ClO-+OH-=SO42-+Cl-+H+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氯气具有强的氧化性,能够氧化二价铁离子;
B.Ca(HCO3)2和NaOH等物质的量反应生成碳酸钙、氢氧化钠和水;
C.酸性的高锰酸钾具有强的氧化性能够氧化双氧水生成氧气;
D.过量SO2通入NaClO,在酸性环境下被氧化生成硫酸和氯化钠.
B.Ca(HCO3)2和NaOH等物质的量反应生成碳酸钙、氢氧化钠和水;
C.酸性的高锰酸钾具有强的氧化性能够氧化双氧水生成氧气;
D.过量SO2通入NaClO,在酸性环境下被氧化生成硫酸和氯化钠.
解答:
解:A.Cl2与FeSO4溶液反应,离子方程式为:Cl2+2Fe2+=2Cl-+2Fe3+,故A正确;
B.等体积、等物质的量浓度的Ca(HCO3)2溶液和NaOH溶液混合,离子方程式:Ca2++HCO3-+OH-=CaCO3↓+H2O,故B正确;
C.用稀硫酸酸化的KMnO4溶液与少量H2O2反应,离子方程式:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O,故C正确;
D.过量SO2通入NaClO溶液中,离子方程式:SO2+ClO-+H2O=SO42-+Cl-+2H+,故D错误;
故选:D.
B.等体积、等物质的量浓度的Ca(HCO3)2溶液和NaOH溶液混合,离子方程式:Ca2++HCO3-+OH-=CaCO3↓+H2O,故B正确;
C.用稀硫酸酸化的KMnO4溶液与少量H2O2反应,离子方程式:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O,故C正确;
D.过量SO2通入NaClO溶液中,离子方程式:SO2+ClO-+H2O=SO42-+Cl-+2H+,故D错误;
故选:D.
点评:本题考查了离子方程式的书写,题目难度不大,明确反应的实质、熟悉离子方程式书写的方法是解题关键,解题时注意反应物用量多少对反应的影响.

练习册系列答案
相关题目
下列实验与对应示意图的关系正确的是( )
A、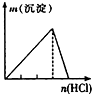 NaAlO2溶液中逐滴滴加稀盐酸至过量 |
B、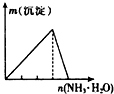 AlCl3溶液中逐滴滴加氨水至过量 |
C、 明矾溶液中逐滴滴加Ba(OH)2至过量 |
D、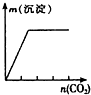 澄清石灰水中缓慢通入CO2至过量 |
下列有关“焰色反应”说法中正确的是( )
| A、非金属单质燃烧时火焰均为无色 |
| B、所有金属及其化合物灼烧时火焰均有颜色 |
| C、NaCl与Na2CO3灼烧时火焰颜色相同 |
| D、焰色反应均应透过蓝色钴玻璃观察 |
以下关于化学实验中“先与后”的说法中正确的是( )
| A、加热试管时,先均匀加热,后集中加热 |
| B、用排水法收集气体后,先撤酒精灯后移出导管 |
| C、制取气体时,先装药品后检验装置气密性 |
| D、称量NaOH固体时,先在托盘上各放两张完全相同的纸,再加药品 |
0.04mol?L-1HCN溶液与0.02mol?L-1 NaOH溶液等体积混合(忽略体积变化),已知混合溶液中c(CN-)<c(Na+),则下列关系中,正确的是( )
| A、c(Na+)>c(CN-)>c(H+)>c(OH-) |
| B、c(HCN)+c(CN-)=0.04 mol?L-1 |
| C、c(Na+)=c(CN-)+c(OH-) |
| D、c(HCN)>c(Na+)>c(CN-) |
分类法在化学的发展中起到非常重要的作用,下列分类标准合理的是( )
| A、根据氧化物的组成元素将氧化物分成酸性氧化物、碱性氧化物和两性氧化物 |
| B、根据反应中是否有化合价变化将化学反应分为氧化还原反应和非氧化还原反应 |
| C、根据分散系是否有丁达尔效应将分散系分为溶液、胶体和浊液 |
| D、根据水溶液能否导电将化合物分为电解质和非电解质 |
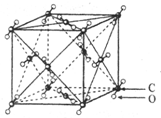 如图为干冰及其晶体的结构模型,下列有关分析正确的是( )
如图为干冰及其晶体的结构模型,下列有关分析正确的是( )| A、构成干冰的微粒是C原子和O原子 |
| B、CO2为极性分子 |
| C、干冰溶于水时有共价键要生成 |
| D、干冰中只存在微弱的分子间作用力 |
瓦斯中甲烷与氧气的质量比为1:4极易爆炸,此时氧气和甲烷的体积比为( )
| A、1:4 | B、1:2 |
| C、1:1 | D、2:1 |
在标准状况下①2.24L CH4 ②3.01×1023个HCl分子 ③0.2mol NH3,下列对这四种气体的关系从大到小表达不正确的是( )
| A、体积②>③>① |
| B、物质的量 ②>③>① |
| C、质量③>②>① |
| D、氢原子个数③>②>① |