题目内容
下列粒子对水的离子平衡不产生影响的是( )
| A、H+ |
| B、Cl- |
| C、NH4+ |
| D、OH- |
考点:水的电离
专题:
分析:酸或碱都抑制水电离,弱离子促进水电离,强酸根离子不促进也不抑制水电离,据此分析解答.
解答:
解:水是弱电解质,在水溶液中存在电离平衡H2O?H++OH-,
A.根据水的电离方程式知,氢离子或氢氧根离子都抑制水电离,故A不选;
B.氯离子不电离出氢离子或氢氧根离子,也不水解,所以不影响水的电离,故B选;
C.铵根离子和氢氧根离子反应生成弱电解质一水合氨,所以促进水电离,故C不选;
D.根据水的电离方程式知,氢离子或氢氧根离子都抑制水电离,故D不选;
故选B.
A.根据水的电离方程式知,氢离子或氢氧根离子都抑制水电离,故A不选;
B.氯离子不电离出氢离子或氢氧根离子,也不水解,所以不影响水的电离,故B选;
C.铵根离子和氢氧根离子反应生成弱电解质一水合氨,所以促进水电离,故C不选;
D.根据水的电离方程式知,氢离子或氢氧根离子都抑制水电离,故D不选;
故选B.
点评:本题考查水的电离,明确弱电解质电离平衡原理是解本题关键,知道哪些物质促进水电离、哪些物质抑制水电离,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
将铁、铝的混合物加入到足量氢氧化钠溶液中,充分反应后过滤,再将过滤得到的固体加入到足量的硫酸铜溶液中,充分反应后过滤得到的固体质量正好与原固体质量相等,则原固体中铝的质量分数为( )
| A、14.3% | B、12.5% |
| C、87.5% | D、无法计算 |
下列说法不正确的是( )
| A、用茚三酮溶液可以鉴别甘氨酸与醋酸 |
| B、中和滴定实验中,用于盛放待测液的锥形瓶洗净后未干燥不会影响测定结果 |
| C、现代仪器分析中,常用质谱仪、元素分析仪、红外光谱仪等测定有机物结构,用原子吸收光谱确定物质中含有哪些非金属元素 |
| D、如果不慎将苯酚沾到皮肤上,应立即用酒精洗涤,再用水冲洗 |
下列物质放置在空气中,不是因为发生氧化还原反应而变质的是( )
| A、Na |
| B、NaCl |
| C、NaOH |
| D、Na2O2 |
已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-?H++B2-,则下列说法中一定正确的是( )
| A、NaHB溶液一定呈酸性,Na2B溶液一定呈碱性 |
| B、Na2B溶液一定呈碱性,NaHB溶液可能呈酸性也可能呈碱性 |
| C、NaHB水溶液中一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+c(B2-) |
| D、在Na2B溶液中一定有:c(OH-)=c(H+)+c(HB-) |
在相同温度时100mL 0.01mol/L的醋酸溶液与10mL 0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是( )
| A、中和时所需NaOH的量 |
| B、电离程度 |
| C、H+的浓度 |
| D、CH3COOH的物质的量 |
对可逆反应N2 (g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,下列叙述正确的是( )
| A、达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
| B、若单位时间内生成x mol N2的同时,消耗2x molNH3,则反应达到平衡状态 |
| C、达到化学平衡时,2v正(H2)=3v逆(NH3) |
| D、加入催化剂,正反应速率增大,逆反应速率不变 |
下列原子(离子)的结构示意图错误的是( )
A、磷原子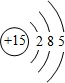 |
B、钠离子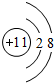 |
C、氧离子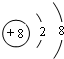 |
D、氢离子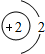 |
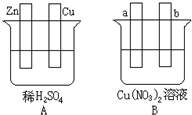 按要求对如图中两极进行必要的联接并填空,a、b为惰性材料.
按要求对如图中两极进行必要的联接并填空,a、b为惰性材料.