题目内容
(6分)将100 mL 5 mol·L-1 NaOH(aq)稀释到500 mL,稀释后溶液中NaOH的物质的量浓度为______________;将氯气通入此溶液充分反应,可制得漂白液,其中含有效成分的物质的量最多为_________________。
1 mol·L-1 ; 0.25 mol 。
【解析】
试题分析:根据方程式Cl2+2NaOH=NaCl+NaClO+H2O计算NaClO的物质的量。100mL 5mol?L-1 NaOH溶液中NaOH的物质的量为0.1L×5mol?L-1=0.5mol,稀释前后NaOH的物质的量不变,则稀释到500mL后溶液中NaOH的物质的量浓度为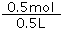 =1mol/L;漂白液的有效成分是NaClO,根据方程式Cl2+2NaOH=NaCl+NaClO+H2O , n(NaClO)=
=1mol/L;漂白液的有效成分是NaClO,根据方程式Cl2+2NaOH=NaCl+NaClO+H2O , n(NaClO)=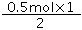 =0.25mol。
=0.25mol。
考点:考查物质的量的相关计算。

练习册系列答案
相关题目
 2HI (g)达到平衡的标志是
2HI (g)达到平衡的标志是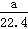 NA
NA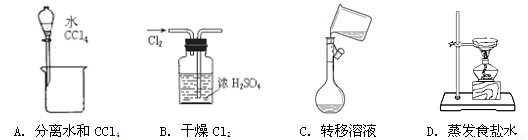

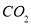 B.
B.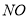
 D.
D.