题目内容
NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A、10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的 质量分数为9.8% |
| B、在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| D、一定温度下,1 L 0.50 mol/L NH4Cl溶液与2 L 0.25 mol/L NH4Cl溶液含NH4+的物质的量相同 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.硫酸密度大于水,加水稀释时密度改变,浓度越小密度越小,以此进行分析;
B.在H2O2+Cl2═2HCl+O2反应中每生成32g氧气,则转移2mol电子;
C.CO、C2H4的分子量都是28,分子数为NA的CO、C2H4混合气体的物质的量为1mol;
D.氯化铵的浓度越小,水解程度越大.
B.在H2O2+Cl2═2HCl+O2反应中每生成32g氧气,则转移2mol电子;
C.CO、C2H4的分子量都是28,分子数为NA的CO、C2H4混合气体的物质的量为1mol;
D.氯化铵的浓度越小,水解程度越大.
解答:
解:A.硫酸密度大于水,加水稀释时密度改变,浓度越小密度越小,10ml质量分数为98%的H2SO4,设密度为x,用水稀释至100ml时密度为y,则x>y,稀释后H2SO4的质量分数约为:
=9.8%×
,由于x>y,则
>1,稀释后的硫酸的质量分数大于9.8%,故A错误;
B.反应中每个氧原子的化合价升高了1价,则每生成32 g氧气,转移2NA个电子,故B正确;
C.CO和C2H4的相对分子质量相等,故无论二者的比例如何,标准状况下的22.4 L气体为1 mol,质量为28 g,故C正确;
D.NH4Cl溶液浓度不同,水解程度不同,因此两种溶液尽管物质的量相同,但所含的NH4+物质的量不同,故D错误;
故选BC.
| x×10×98% |
| 100×y |
| x |
| y |
| x |
| y |
B.反应中每个氧原子的化合价升高了1价,则每生成32 g氧气,转移2NA个电子,故B正确;
C.CO和C2H4的相对分子质量相等,故无论二者的比例如何,标准状况下的22.4 L气体为1 mol,质量为28 g,故C正确;
D.NH4Cl溶液浓度不同,水解程度不同,因此两种溶液尽管物质的量相同,但所含的NH4+物质的量不同,故D错误;
故选BC.
点评:本题考查阿伏加德罗常数的应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,选项B为易错点,注意双氧水中氧元素的化合价为-1价.

练习册系列答案
相关题目
下列说法正确的是( )
| A、C6H5CH2OH不属于醇类 |
| B、l mol苯最多能与3 mol H2加成,说明每个苯分子有3个碳碳双键 |
| C、苯和甲苯都能使KMnO4酸性溶液褪色 |
| D、1-氯丙烷和2-氯丙烷分别与NaOH乙醇溶液共热的反应产物相同 |
下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是( )
| A、Cu与浓硝酸反应比稀硝酸反应快 |
| B、Cu能与浓硝酸反应,而不与浓盐酸反应 |
| C、N2与O2在常温、常压下不反应,放电时可反应 |
| D、Cu与浓硫酸能反应,而不与稀硫酸反应 |
下列装置中电流表指针会发生偏转的是( )
A、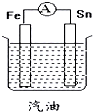 |
B、 |
C、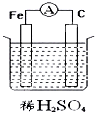 |
D、 |
向纯水中加入少量NaHSO4晶体,若温度不变,则溶液中( )
| A、水电离出的H+大于水电离出的OH-浓度 |
| B、c(H+).c(OH-)乘积增大 |
| C、酸性增强 |
| D、H+,OH-浓度均增大 |
已知:HCl为强酸,下列对比实验不能用于证明CH3COOH为弱酸的是( )
| A、对比等浓度的两种酸的pH |
| B、对比等浓度的两种酸,与相同大小镁条反应的初始速率 |
| C、对比等浓度、等体积的两种酸,与等量NaOH溶液反应后放出的热量 |
| D、对比等浓度、等体积的两种酸,与足量Zn反应,生成H2的体积 |
一种新型燃料电池,它是用惰性金属作电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气,发生的电极反应为:X极:CH4+10OH--8e-=CO32-+7H2O Y极:2O2+4H2O+8e-=8OH-;关于此燃料电池的说法不正确的是( )
| A、该电池工作时通甲烷一极附近溶液的pH升高 |
| B、工作一段时间后,KOH的物质的量减少 |
| C、X极发生氧化反应,Y极发生还原反应 |
| D、在标准状况下通入5.6 L O2完全反应,则有1 mol电子发生转移 |
将100ml、0.1mol/L的BaCl2溶液中加入到100ml、0.2mol/L的H2SO4溶液中,则溶液中存在的离子浓度的关系的是( )
| A、[H+]>[Cl-]>[Ba2+]>[SO42-] |
| B、[Cl-]>[H+]>[SO42-]>[Ba2+] |
| C、[H+]>[Cl-]>[SO42-]>[Ba2+] |
| D、[Cl-]>[H+]>[Ba2+]>[SO42-] |