题目内容
18.如图所示分离混合物时常用的仪器,从左至右,对应的混合物分离操作方法正确的是( )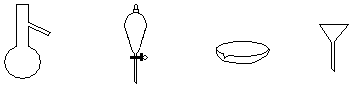
| A. | 蒸发、过滤、蒸馏、分液 | B. | 蒸馏、分液、蒸发、过滤 | ||
| C. | 蒸馏、过滤、蒸发、分液 | D. | 蒸发、分液、蒸馏、过滤 |
分析 由图可知,仪器分别为蒸馏烧瓶、分液漏斗、蒸发皿、漏斗,以此来解答.
解答 解:由图可知,仪器分别为蒸馏烧瓶、分液漏斗、蒸发皿、漏斗,
蒸馏烧瓶用于蒸馏实验;
分液漏斗用于分层液体混合物的分离,可分液;
蒸发皿用于分离可溶性固体,蒸发分离混合物;
过滤用于分离不溶性固体与溶液,需要漏斗,
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握仪器的使用、混合物分离提纯实验为解答的关键,侧重分析与实验能力的考查,注意实验基本操作,题目难度不大.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
9.如图为用含少量铁的废铜渣为原料生产胆矾的流程:

金属离子沉淀的pH
(1)写出浸出时铜与稀硝酸反应的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(2)在浸出时加入稀硫酸的作用提供酸性环境,使NO3-氧化铜
(3)试剂b为CuO或Cu(OH)2;滤渣c为Fe(OH)3.
(4)取样检验是为了证明没有Fe3+存在,其方法是向试样中滴加KSCN溶液,无明显现象.
(5)从滤液中得到胆矾的操作是蒸发浓缩、冷却结晶、过滤
(6)气体 a 可以被循环利用,用化学方程式表示气体 a 被循环利用的原理为2NO+O2=2NO2、3NO2+H2O=2HNO3+NO.
(7)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和 O2气体,且n (SO3):n (SO2)=1:2,写出硫酸铜受热分解的化学方程式3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑.

金属离子沉淀的pH
| 离子种类 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
(2)在浸出时加入稀硫酸的作用提供酸性环境,使NO3-氧化铜
(3)试剂b为CuO或Cu(OH)2;滤渣c为Fe(OH)3.
(4)取样检验是为了证明没有Fe3+存在,其方法是向试样中滴加KSCN溶液,无明显现象.
(5)从滤液中得到胆矾的操作是蒸发浓缩、冷却结晶、过滤
(6)气体 a 可以被循环利用,用化学方程式表示气体 a 被循环利用的原理为2NO+O2=2NO2、3NO2+H2O=2HNO3+NO.
(7)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和 O2气体,且n (SO3):n (SO2)=1:2,写出硫酸铜受热分解的化学方程式3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑.
6.NA代表阿伏伽德罗常数,下列说法正确的是( )
| A. | 1.4g乙烯和丙烯混合气体中含有C-H键的数目为0.2NA | |
| B. | 0.10molFe粉与足量水蒸气反应生成的H2分子数为0.10NA | |
| C. | 标准状况下,11.2LCO2与足量Na2O2反应,转移的电子数为NA | |
| D. | 若将1mol氧化铁完全转化为氢氧化铁胶体,则分散系中胶体粒子数为NA |
13.在自然界中不存在游离态的元素是( )
| A. | 碳 | B. | 硫 | C. | 铁 | D. | 铝 |
3.下列四个反应(条件略,已配平),酸所体现的性质与其他三者有所不同的是( )
| A. | MnO2+4HCl(浓)→MnCl2+Cl2↑+2H2O | |
| B. | Ag+2HNO3(浓)→AgNO3+NO2↑+H2O | |
| C. | C+2H2SO4(浓)→CO2↑+2SO2↑+2H2O | |
| D. | 3Fe3O4+28HNO3(浓)→9Fe(NO3)3+NO↑+14H2O |
10.给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
| A. | S$→_{点燃}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | Al2O3$→_{△}^{NaOH}$NaAlO2(ap)$\stackrel{CO_{2}}{→}$Al(OH)3(s) | |
| C. | Fe$→_{高温}^{H_{2}O}$Fe2O3$\stackrel{盐酸}{→}$FeCl3(ap) | |
| D. | Cu$→_{H_{2}SO_{4},△}^{O_{2}}$CuSO4(ap)$→_{△}^{过量NaOH(ap),葡萄糖}$CuO(s) |
7.下列有关实验操作、现象、解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,排水法收集气体 | HX放出的氢气多 | HX酸性比HY弱 |
| B | 先向2mL0.15mol•L-1 Na2S溶液中滴几滴0.15mol•L-1 ZnSO4溶液,再加入几滴0.1mol•L-1 CuSO4溶液 | 开始有白色沉淀生成;后又有黑色沉淀生成 | Ksp(ZnS)<Ksp(CuS) |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 向紫色石蕊试液中持续长时间通入氯气 | 溶液先变红,最后变为无色 | 氯气有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
8.利用微生物电池除去废水中的乙酸钠和氯苯,其原理如图所示,下列说法错误的是( )
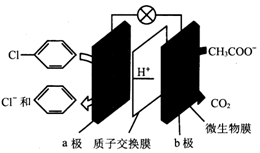

| A. | 该装置能将化学能转化为电能 | |
| B. | a极发生还原反应 | |
| C. | b极电极反应为CH3COO-+2H2O-8e-═2CO2↑+7H+ | |
| D. | 每除去1mol氯苯,电路中转移1mol电子 |
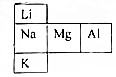 试分析它们的原子结构(电子层数、最外层电子)请指出:
试分析它们的原子结构(电子层数、最外层电子)请指出: