题目内容
已知25℃、101kPa下,如右图所示,石墨的燃烧热为393.5kJ/mol,金刚石的燃烧热为395.0kJ/mol 。下列说法或表达正确的是:
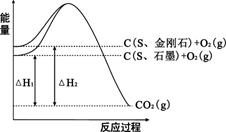
A.金刚石比石墨稳定
B.C(s、石墨)=C(s、金刚石) △H =+1.5kJ/mol
C.△H1<△H2
D.如果使用催化剂,△H1和△H2都变小
【答案】
B
【解析】
试题分析:A选项中,金刚石能量更高所以更不稳定,石墨比金刚石稳定。B选项中△H=395.0kJ/mol—393.5kJ/mol=+1.5kJ/mol;C选项中由于金刚石的能量比石墨高,所以△H2<△H1,△H为负值。D选项中催化剂只改变反应的活化能,不会改变物质原本的能量。
考点:化学反应能量的变化
点评:数形结合进行分析,属于简单题。

练习册系列答案
相关题目