题目内容
19.下列能说明碳与氮两元素非金属性相对强弱的是( )| A. | 相同条件下水溶液的pH:Na2CO3>Na2SO4 | |
| B. | 酸性:H2SO3>H2CO3 | |
| C. | CH4比NH3更稳定 | |
| D. | C与H2的化合价比N2与H2的化合更容易 |
分析 A.最高价氧化物的水化物的酸性越强,元素的非金属性越强;
B.最高价氧化物的水化物的酸性越强,元素的非金属性越强;
C.氢化物越稳定,其元素的非金属性越强;
D.与氢气化合越容易,元素的非金属性越强.
解答 解:A.相同条件下水溶液的pH:Na2CO3>Na2SO4,说明碳酸的酸性强于硫酸,碳酸和硫酸为C和S元素的最高价氧化物对应的水化物,则证明非金属性S>C,故A正确;
B.酸性:H2SO3>H2CO3,由于亚硫酸不是S元素的最高价氧化物对应的水化物,无法比较二者的非金属性大小,故B错误;
C.氢化物越稳定,其元素的非金属性越强,NH3比CH4更稳定,故C错误;
D.C与H2的化合比N2与H2的化合更困难,故D错误.
故选:A.
点评 本题考查了元素非金属性强弱比较,题目难度不大,注意把握非金属性强弱比较的方法,侧重于基础知识的考查,注意对规律的归纳整理,题目难度不大.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
9.为探究Cl2、漂白粉的制备及有关性质,某兴趣小组设计并进行了以下实验探究.请回答以下问题:
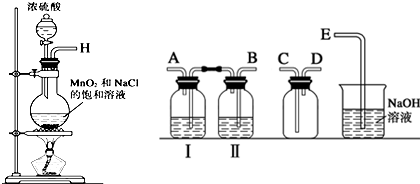
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:H→B、A→C、D→E;其中广口瓶Ⅱ中的试剂为饱和食盐水.
(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)实验室有一瓶密封不严的漂白粉样品,其中肯定存在CaCl2.请设计实验,探究该样品中除CaCl2外还含有的其他固体物质.
①提出合理假设.
假设1:该漂白粉未变质,还含有Ca(ClO)2
假设2:该漂白粉全部变质,还含有CaCO3;
假设3:该漂白粉部分变质,还含有Ca(ClO)2和CaCO3.
②设计实验方案,进行实验.请在下表中写出实验步骤、预期现象和结论.
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、品红溶液、1mol•L-1 HCl溶液、新制澄清石灰水.(提示:不必检验Ca2+和Cl-.)
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:H→B、A→C、D→E;其中广口瓶Ⅱ中的试剂为饱和食盐水.

(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)实验室有一瓶密封不严的漂白粉样品,其中肯定存在CaCl2.请设计实验,探究该样品中除CaCl2外还含有的其他固体物质.
①提出合理假设.
假设1:该漂白粉未变质,还含有Ca(ClO)2
假设2:该漂白粉全部变质,还含有CaCO3;
假设3:该漂白粉部分变质,还含有Ca(ClO)2和CaCO3.
②设计实验方案,进行实验.请在下表中写出实验步骤、预期现象和结论.
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、品红溶液、1mol•L-1 HCl溶液、新制澄清石灰水.(提示:不必检验Ca2+和Cl-.)
| 实验步骤 | 预期现象与结论 | |
| 步骤1 | 取少量上述漂白粉于试管中,先加入适量1mol•L-1盐酸溶解后,再把生成的气体通入新制澄清石灰水中. | 若澄清石灰水未见浑浊,则假设1成立; 若澄清石灰水变浑浊,则假设2或假设3成立. |
| 步骤2 | 已确定漂白粉变质,则另取少量上述漂白粉于试管中,先加入适量1mol•L-1 HCl溶液,再加入几滴品红溶液振荡. | 若品红溶液不褪色,则假设2成立; 若品红溶液褪色,则假设3成立. |
7.如图为元素周期表的一部分,下列有关短周期元素X,Y,Z,R的叙述正确的是( )

| A. | 热稳定性:Y的气态氢化物>Z的气态氢化物 | |
| B. | Z的最高价氧化物对应水化物的分子式为H2ZO4 | |
| C. | X元素的单质能与所有强酸发生反应放出H2 | |
| D. | R的核外电子数与OH-的核外电子数相同 |
14.已知: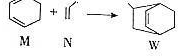 下列说法正确的是( )
下列说法正确的是( )
 下列说法正确的是( )
下列说法正确的是( )| A. | W的分子式为C9H12 | |
| B. | N分子的所有原子在同一平面上 | |
| C. | M的二氯代物有8种(不考虑立体异构) | |
| D. | M、N、W均可发生氧化反应、还原反应和加聚反应 |
4.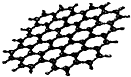 最近,科学家从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质.可以制成纳米材料.其结构如图所示:下列关于石墨烯的说法正确的是( )
最近,科学家从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质.可以制成纳米材料.其结构如图所示:下列关于石墨烯的说法正确的是( )
 最近,科学家从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质.可以制成纳米材料.其结构如图所示:下列关于石墨烯的说法正确的是( )
最近,科学家从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质.可以制成纳米材料.其结构如图所示:下列关于石墨烯的说法正确的是( )| A. | 属于高分子化合物 | B. | 与金刚石互为同分异构体 | ||
| C. | 性质稳定不能与氧气等物质反应 | D. | 能导电 |
6.化学是一门与社会、生活、科研密切相关的自然科学.下列有关叙述中,不正确的是( )
| A. | 利用化学反应可实现12C到14C的转化 | |
| B. | 天然气、煤气大量泄漏遇到明火会爆炸 | |
| C. | 大量使用燃煤发电是形成雾霾的主要原因 | |
| D. | 晶体硅可用作半导体材料 |
4.下列关于物质检验的说法中正确的是( )
| A. | 往某溶液中滴加BaCl2溶液,产生白色沉淀,则原溶液中一定含SO42- | |
| B. | 往某溶液中滴加稀硝酸酸化的硝酸银溶液,产生白色沉淀,则原溶液中一定含Cl- | |
| C. | 取某溶液进行焰色反应,透过蓝色钴玻璃焰色为紫色,则原溶液的溶质一定是钾盐 | |
| D. | 往某溶液中通入CO2,产生白色沉淀,则原溶液中一定含SiO32- |