题目内容
(6分)在一定体积的密闭容器中,进行如下化学反应:
C(s)+H2O(g)  CO(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
t/(℃) | 700 | 800 | 830 | 1000 | 1200 |
K | 0.7 | 0.8 | 1.0 | 1.6 | 2.4 |
(1)该反应的化学平衡常数表达式为K=____ ____,该反应为________反应(填“吸热”或“放热”)。
(2)能作为判断反应达到化学平衡状态的依据是________。
A.容器中压强不变 B.c(H20)不变
C.v正(H2)=v逆(H2O) D.c(H2)=c(CO)
(3)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,缩小容器的体积,平衡________移动(填“正向”、“逆向”或“不”)。H2O(g)的浓度___ ____,CO(g)的浓度___ ____(填“变大”、“不变”或“变小”)
(1) K=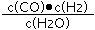 ,吸热反应。(2)ABC (3)逆向 。变大,变大
,吸热反应。(2)ABC (3)逆向 。变大,变大
【解析】
试题分析:(1)因平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以K=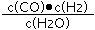 ,化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热;
,化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热;
(2)A、反应后气体的物质的量增加,温度一定,容器中压强增大,所以当压强不变时,说明到达平衡状态,A正确;B、反应后气体的物质的量增加,气体的质量增大,混合气体的平均相对分子质量改变,所以当混合气体的平均相对分子质量不再变化,说明到达平衡状态,B正确;C、v (H2)正=v (H2O)逆不同物质表示的速率之比等于化学计量数之比,说明到达平衡状态,C正确;D、平衡时氢气的浓度与一氧化碳的浓度与转化率有关,所以c(H2)=c(CO)不能说明到达平衡,D错误;
(3)其他条件不变的情况下,缩小容器的体积,压强增大,正反应为气体体积增大的反应,故平衡向逆反应移动;由于平衡移动引起的浓度变化小于因体积减小引起的浓度变化,所以容器的体积减小,反应物和生成物浓度均变大;
考点:考查化学反应速率、化学平衡原理和化学平衡常数。

 小学教材完全解读系列答案
小学教材完全解读系列答案 2NO(g)+O2(g),在容积固定的密闭容器中,达到平衡状态的标志是
2NO(g)+O2(g),在容积固定的密闭容器中,达到平衡状态的标志是