题目内容
难溶化合物的饱和溶液存在着溶解平衡,例如:AgCl(s)?Ag++Cl-.[已知Ksp(AgCl)=1.8×10-10]
(1)向50mL 0.018mol/L的 AgNO3溶液中加入50mL 0.02mol/L的盐酸,沉淀生成后溶液中c(Ag+)是 mol/L.
(2)如果向生成沉淀后的溶液中再加入50mL 0.001mol/L的盐酸,是否产生沉淀 (填“是”或“否”).
(1)向50mL 0.018mol/L的 AgNO3溶液中加入50mL 0.02mol/L的盐酸,沉淀生成后溶液中c(Ag+)是
(2)如果向生成沉淀后的溶液中再加入50mL 0.001mol/L的盐酸,是否产生沉淀
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)依据题干数据计算沉淀后溶液中氯离子浓度,结合Ksp计算溶液中银离子浓度;
(2)根据溶液中c(Ag+)?c(Cl-)与Ksp的大小关系分析.
(2)根据溶液中c(Ag+)?c(Cl-)与Ksp的大小关系分析.
解答:
解:(1)向50ml0.018mol/L的AgNO3溶液中加入50ml0.02mol/L的盐酸,混合后两者浓度分别为c(Ag+)=
mol/L=0.009 mol/L、c(Cl-)=
mol/L=0.01mol/L,Ag+与Cl-是等物质的量反应的,此时Cl-过量,过量浓度c(Cl-)=0.01-0.009=0.001mol/L,
Ksp=c(Ag+)×C(Cl-)=1.8×10-10,则:c(Ag+)=
=1.8×10-7mol/L,
答:沉淀生成后溶液中c(Ag+)是1.8×10-7mol/L;
(2)向沉淀生成后的溶液中再加入50mL0.001mol/L的盐酸,则溶液体积为0.15L,
c(Ag+)=
×0.1=1.2×10-7mol/L,c(Cl-)=0.001mol/L,
则c(Ag+)?c(Cl-)=1.2×10-7×0.001=1.2×10-10<Ksp=1.8×10-10,所以不产生沉淀,
答:不产生沉淀,因为在溶液中c(Ag+)?c(Cl-)<Ksp,溶液未饱和.
| 0.018 |
| 2 |
| 0.02 |
| 2 |
Ksp=c(Ag+)×C(Cl-)=1.8×10-10,则:c(Ag+)=
| 1.8×10-10 |
| 0.001 |
答:沉淀生成后溶液中c(Ag+)是1.8×10-7mol/L;
(2)向沉淀生成后的溶液中再加入50mL0.001mol/L的盐酸,则溶液体积为0.15L,
c(Ag+)=
| 1.8×10-7 |
| 0.15 |
则c(Ag+)?c(Cl-)=1.2×10-7×0.001=1.2×10-10<Ksp=1.8×10-10,所以不产生沉淀,
答:不产生沉淀,因为在溶液中c(Ag+)?c(Cl-)<Ksp,溶液未饱和.
点评:本题考查溶液浓度的计算,本题难度不大,做题时注意判断两种物质的反应程度,再根据溶度积常数计算.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列对沉淀溶解平衡的描述不正确的是( )
| A、用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| B、物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的 |
| C、除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大 |
| D、沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全 |
下列说法中正确的是( )
| A、增大反应物浓度,可逆反应正速率增大;减少反应物浓度,可逆反应逆速率增大 |
| B、粗铜精炼时,电解质液中的c(Cu2+)保持不变 |
| C、纯银在空气中久置变黑发生的是电化学腐蚀 |
| D、阴极电保护法是将被保护的金属与外加电源的负极相连 |
如图所示,装置在常温下工作(溶液体积变化忽略不计).闭合K,灯泡发光.下列叙述中不正确的是( )
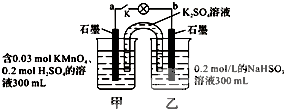

| A、当电路中有1.204×1022个电子转移时,乙烧杯中溶液的C(H+)约为0.1mol?L-1 |
| B、电池工作时,盐桥中的K+移向甲烧杯 |
| C、电池工作时,外电路的电子方向是从a到b |
| D、乙池中的氧化产物为SO42- |
气体A、B分别为0.6mol和0.5mol,在0.4L密闭容器中发生反应:3A+B?aC+2D,经5min后,此时C为0.2mol,又知在此反应时间内,D的平均反应速率为0.1mol?(L?min)-1,下列结论正确的是( )
| A、此时,反应混合物总的物质的量为1mol |
| B、B的转化率为50% |
| C、A的平均反应速率为0.1mol?(L?min)-1 |
| D、a值为2 |

