题目内容
写出下列反应的反应方程式
(1)乙醇与氧气(铜做催化剂):
(2)乙醇与乙酸: .
(1)乙醇与氧气(铜做催化剂):
(2)乙醇与乙酸:
考点:化学方程式的书写,乙醇的化学性质
专题:有机物的化学性质及推断
分析:(1)乙醇在Cu做催化剂加热时与氧气反应,被氧化生成乙醛和水;
(2)发生酯化反应生成乙酸乙酯和水.
(2)发生酯化反应生成乙酸乙酯和水.
解答:
解:(1)乙醇在Cu做催化剂加热时与氧气反应,被氧化生成乙醛和水,方程式为2CH3CH2OH+O2
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;
(2)乙酸能够与乙醇发生酯化反应生成乙酸乙酯和水,反应的化学方程式为CH3COOH+HOC2H5
CH3COOC2H5+H2O,故答案为:CH3COOH+HOC2H5
CH3COOC2H5+H2O.
| Cu |
| △ |
| Cu |
| △ |
(2)乙酸能够与乙醇发生酯化反应生成乙酸乙酯和水,反应的化学方程式为CH3COOH+HOC2H5
| 浓H2SO4 |
| △ |
| 浓H2SO4 |
| △ |
点评:本题考查有机化学反应方程式的书写,为高频考点,把握官能团与性质的关系为解答的关键,侧重常见有机物性质及反应类型的考查,注意有机反应的条件,题目难度不大.

练习册系列答案
相关题目
下列反应中,铁元素被氧化的是( )
| A、FeS+2HCl=FeCl2+H2S↑ |
| B、Fe+H2SO4=FeSO4+H2↑ |
| C、FeO+2HCl=FeCl2+H2O |
| D、2FeCl3+Cu=2FeCl2+CuCl2 |
设阿伏加德罗常数为NA,标准状况下O2和N2的混合气体mg,含有b个分子,则ng该混合气体在相同状况下所占的体积(L)应是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol NH4+ 所含质子数为10NA |
| B、10 g氖气所含原子数约为6.02×1023 |
| C、22.4 L SO2所含的分子数为NA |
| D、常温常压下,32 g O2所含原子数为2NA |
下列反应的离子方程式中错误的是( )
| A、氯化铝溶液中加入过量的氨水Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| B、用醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、将铜屑加入Fe3+溶液中:Fe3++Cu=Fe2++Cu2+ |
| D、将铝片放入过量NaOH溶液中2Al+2OH-+2H2O=2AlO2-+3H2↑ |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、常温常压下,2.8g N2与C2H4的混合气体所含电子数为1.4 NA |
| B、标准状况下,1.12LNO与1.12O2的混合物中含有的原子数为0.2NA |
| C、Na2O2与H2O反应生成1.12LO2(标准状况),反应中转移的电子数为0.2NA |
D、32gS8单质中含有的S-S键个数为2NA |
标准状况下,下列物质的体积最大的是( )
| A、0.3mol的NH3 |
| B、18g水 |
| C、2mol的Al (密度约2.7g/cm3 ) |
| D、1.204×1023个HCl分子 |
下列离子方程式的书写正确的是( )
| A、铝与盐酸反应:Al+6H+═Al3++3H2↑ |
| B、少量CO2通入Ca(OH)2溶液中:CO2+2OH-═CO32-+H2O |
| C、氢氧化钠溶液与盐酸反应:NaOH+H+═H2O+Na+ |
| D、碳酸钠与氯化钙混合:CO32-+Ca2+═CaCO3↓ |
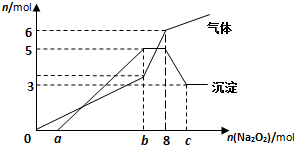 将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的
将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的
Mg2+、Al3+、NH4+物质的量分别为( )
| A、2mol、3mol、6mol |
| B、3mol、2mol、6mol |
| C、2mol、3mol、4mol |
| D、3mol、2mol、2mol |