题目内容
12. 某化学学习小组的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x的值.该组同学通过查阅资料查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
某化学学习小组的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x的值.该组同学通过查阅资料查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
学习小组的同学设计了滴定的方法测定x值.
①称取1.260g纯草酸晶体,将其制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol/L的酸性KMnO4标准溶液进行滴定,达到终点时消耗了10.00mL.
请回答下列问题:
(1)配制100.00mL待测液时,使用的玻璃仪器除烧杯、玻璃棒及胶头滴管外,还需要100mL容量瓶.
(2)滴定时,将酸性KMnO4标准液装在如图中的甲(填“甲”或“乙”)滴定管中.本实验滴定达到终点的标志是当滴入最后一滴酸性KMnO4溶液时,溶液由无色变为浅紫色,且半分钟内不褪色.
(3)通过上述数据,求得x=2.
(4)讨论:
①若滴定终点时俯视滴定管,则由此测得的x值会偏大(填“偏大”、“偏小”或“不变”,下同).
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会偏小.
分析 (1)配制100.00mL溶液时,需要的玻璃仪器有烧杯、玻璃棒、100mL容量瓶、胶头滴管;
(2)酸性溶液盛放在酸式滴定管中,碱性溶液盛放在碱性滴定管中;
酸性高锰酸钾溶液呈紫色,草酸和酸性高锰酸钾溶液发生氧化还原反应而使酸性高锰酸钾溶液褪色;
(3)由题给化学方程式:2MnO4-+5H2C2O4+6H+?2Mn2++10CO2↑+8H2O及数据可知,1.260g纯草酸晶体中含H2C2O4的物质的量为:0.1000 mol/L×10.00 mL×10-3 L/mL×$\frac{5}{2}$×$\frac{100mL}{25mL}$=0.0100 mol,则1.260gH2C2O4•xH2O中含H2O的物质的量为$\frac{1.260g-0.0100mol×90g/mol}{18g/mol}$=0.020 0 mol,根据草酸和水的物质的量之比确定x值;
(4)根据c(待测)=$\frac{c(标准).V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差,从而判断对测得的x值的影响.
解答 解:(1)配制100.00mL溶液时,需要的玻璃仪器有烧杯、玻璃棒、100mL容量瓶、胶头滴管,所以还需要的仪器是100mL容量瓶,故答案为:100mL容量瓶;
(2)酸性高锰酸钾溶液呈酸性,应该用酸式滴定管甲盛放;酸性高锰酸钾溶液呈紫色,草酸和酸性高锰酸钾溶液发生氧化还原反应而使酸性高锰酸钾溶液褪色,则终点现象为当滴入最后一滴酸性KMnO4溶液时,溶液由无色变为浅紫色,且半分钟内不褪色,
故答案为:甲;当滴入最后一滴酸性KMnO4溶液时,溶液由无色变为浅紫色,且半分钟内不褪色;
(3)由题给化学方程式:2MnO4-+5H2C2O4+6H+?2Mn2++10CO2↑+8H2O及数据可知,1.260g纯草酸晶体中含H2C2O4的物质的量为:0.1000 mol/L×10.00 mL×10-3 L/mL×$\frac{5}{2}$×$\frac{100mL}{25mL}$=0.0100 mol,则1.260gH2C2O4•xH2O中含H2O的物质的量为$\frac{1.260g-0.0100mol×90g/mol}{18g/mol}$=0.020 0 mol,草酸和水的物质的量之比等于其计量数之比=0.0100mol:0.0200mol=1:2,所以x=2,
故答案为:2;
(4)①若滴定终点时俯视滴定管刻度,造成V(标准)偏小,根据c(待测)=$\frac{c(标准).V(标准)}{V(待测)}$知,c(待测)偏小,由此所得n(H2C2O4)偏小,则n(H2O)偏大,x偏大,
故答案为:偏大;
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,造成V(标准)偏大,根据c(待测)=$\frac{c(标准).V(标准)}{V(待测)}$知,c(待测)偏大,由此所得n(H2C2O4)偏大,则n(H2O)偏小,x偏小,
故答案为:偏小.
点评 本题以滴定实验为载体考查物质组成,侧重考查学生实验操作、实验分析及判断能力,明确实验原理、实验操作规范性和方法是解本题关键,难点是误差分析,注意量筒和滴定管俯视时读数误差区别,为易错点,

 阅读快车系列答案
阅读快车系列答案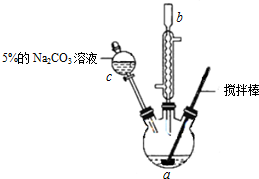
Ⅰ.实验步骤如下:
①向三颈瓶中依次加入:10.0mL丙烯酸(CH2=CHCOOH)、适量的浓硫酸、10.0mL无水甲醇、
2粒沸石,按图示装置连接好冷凝管,用搅拌棒搅拌,水浴加热.
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性.
③分液,取上层油状液体,再用无水Na2SO4干燥后蒸馏,收集70℃~90℃馏分.
可能用到的信息:
| 密度 | 沸点 | 溶解性 | ||
| 丙烯酸 | 1.05g/cm3 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
| 甲醇 | 0.79g/cm3 | 64.7℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
| 丙烯酸甲酯 | 0.95g/cm3 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
(1)仪器c的名称是分液漏斗.
(2)混合液用5% Na2CO3溶液洗涤的作用是除去丙烯酸、浓硫酸等酸性物质.
(3)该实验中应采用的安全防护措施有通风橱中实验.(1条即可)
Ⅱ.为测定上述反应中丙烯酸甲酯的产率,设计如下实验:
①将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol/L的KOH溶液10.0mL,加热使之完全水解.
②用酚酞做指示剂,向冷却后的溶液中滴加0.5mol/L的HCl溶液,中和过量的KOH,滴到终点时共消耗盐酸20.00mL.
(4)请写出(Ⅱ)操作①中发生的化学反应方程式CH2=CHCOOCH3+KOH$\stackrel{△}{→}$CH2=CHCOOK+CH3OH.
(5)计算本次酯化反应丙烯酸甲酯的产率.
I.配制100mL 0.10mol/L NaOH标准溶液.
II.取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准
NaOH溶液进行滴定.
III.重复上述滴定操作2~3次,记录数据如下.
| 实验 编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测HCl溶液的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
(2)根据上述数据,可计算出该盐酸的浓度约为0.11mol/L(保留两位有效数字).
(3)排去碱式滴定管中气泡的方法应采用如图丙的操作,然后挤压玻璃球使尖嘴部分充满碱液.

(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有EF(多选扣分).
A.滴定终点读数时俯视读数 B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥 D.配制NaOH标准溶液时,没有等溶解液降至室温就转移至容量瓶中
E.配制NaOH标准溶液时,定容时仰视容量瓶的刻度线
F.碱式滴定管尖嘴部分有气泡,滴定后消失.
| A. | 不发生反应 | B. | 铁被钝化 | C. | 产生大量SO2 | D. | 产生大量H2 |
 某化学学习小组的同学 依据氧化还原反应:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O,可采用滴定的方法测定FeSO4的质量分数,实验步骤如下:
某化学学习小组的同学 依据氧化还原反应:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O,可采用滴定的方法测定FeSO4的质量分数,实验步骤如下: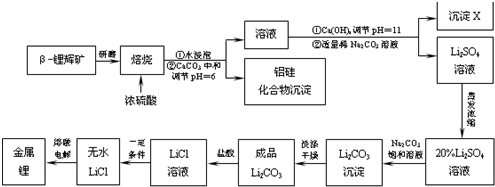

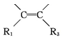 $→_{(2)Zn/H_{2}O}^{(1)O_{2}}$R1CHO+
$→_{(2)Zn/H_{2}O}^{(1)O_{2}}$R1CHO+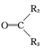
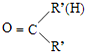 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$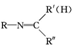 +H2O
+H2O  +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O
+H2O .
.  (写出其中一种的结构简式).
(写出其中一种的结构简式).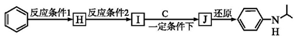 ,
, .
.