题目内容
【题目】一位同学为探究元素周期表中元素性质的递变规律,设计了如下列实验.
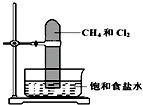
(1)根据题意解答 (i)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:与盐酸反应最剧烈,与盐酸反应的速度最慢;与盐酸反应产生的气体最多.
(ii)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为 .
(2)利用如图装置可验证同主族元素非金属性的变化规律: 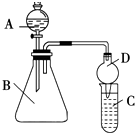
(i)仪器B的名称为 , 干燥管D的作用为 .
(ii)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液的现象,即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用溶液吸收尾气.
(iii)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有溶液的洗气瓶除去.
【答案】
(1)钾;铝;铝;S2﹣+Cl2═S↓+2Cl﹣
(2)锥形瓶;防止倒吸;变蓝;NaOH;有白色沉淀生成;饱和NaHCO3
【解析】解:(1)(i)金属活泼性顺序为:钾>钠>镁>铝,所以相同条件下与盐酸反应最激烈的是钾,反应速率最慢的是铝;生成1mol氢气需要得到2mol电子,1mol钾、钠都失去1mol电子,1mol镁失去2mol电子,而1mol铝失去3mol电子,所以生成氢气最多的是金属铝,所以答案是:钾;铝;铝; (ii)氯气氧化性强于硫单质,所以氯气能够与硫离子反应生成硫,反应的离子方程式为:S2﹣+Cl2═S↓+2Cl﹣ , 所以答案是:S2﹣+Cl2═S↓+2Cl﹣;(2)(i)仪器B为锥形瓶;球形干燥管D能够防止倒吸,可以避免C中液体进入锥形瓶中,所以答案是:锥形瓶;防止倒吸; (ii)KMnO4与浓盐酸常温下反应生成氯气,氯气能够将碘离子氧化成碘单质,碘单质遇到淀粉变成蓝色,氯气是一种有毒气体,必须进行尾气吸收,氯气能够与氢氧化钠溶液反应,可以使用氢氧化钠溶液吸收多余的氯气, 所以答案是:变蓝;NaOH;(iii)氯化氢具有挥发性,干扰实验结果,需要将二氧化碳中的氯化氢除掉,根据氯化氢与碳酸氢钠反应,而二氧化碳不反应,可以在B和C之间增加装有饱和NaHCO3溶液的洗气瓶,所以答案是:有白色沉淀生成;饱和NaHCO3 .
【考点精析】解答此题的关键在于理解非金属在元素周期表中的位置及其性质递变的规律的相关知识,掌握在目前已知的112种元素中,非金属元素有22种,除H外非金属元素都位于周期表的右上方(H在左上方).F是非金属性最强的元素.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑨九种元素在周期表中的位置.
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ |
请回答:
(1)以上元素中,最高价氧化物对应水化物酸性最强的是;碱性最强的是;显两性的是(填化学式)
(2)③、④、⑨三种元素按原子半径由大到小的顺序依次为(填元素符号)
(3)按要求写出下列两种物质的电子式:⑥的氢化物; ⑨的最高价氧化物的对应的水化物;
(4)由H和①形成的原子数之比为1:1的物质(填化学式).
(5)利用⑧的单质制备漂白粉发生反应的化学方程式为 .
(6)⑤的最高价氧化物对应的水化物既能与③的最高价氧化物对应的水化物反应,也能与⑧的最高价氧化物对应的水化物反应.分别写出其反应的离子方程式是; .