题目内容
2.煤样1.000g,经高温氧气流中燃烧,使其中各种硫化物均转化为SO2及SO3,然后用H2O2溶液吸收使之生成H2SO4.生成的H2SO4用NaOH标准溶液[c(NaOH)=0.05012mool/L]滴定,用去8.00mL,计算煤样中硫的质量分数.SO2+SO3+H2O2+H2O=2H2SO4
H2SO4+2NaOH=Na2SO4+2H2O.
分析 根据反应方程式H2SO4+2NaOH=Na2SO4+2H2O计算出参加反应的硫酸的物质的量,根据S元素守恒可以推出原煤样中的S元素的质量,进而可以计算出煤样中硫的质量分数.
解答 解:n(NaOH)=C(NaOH)×V=0.05012mol/L×8×10-3L=4×10-4mol
H2SO4+2NaOH=Na2SO4+2H2O
1 2
n(H2SO4)4×10-4mol
n(H2SO4)=2×10-4mol
根据硫元素守恒可知:n(S)=n(H2SO4)=2×10-4mol
m(S)=n(S)×M(S)=2×10-4mol×32g/mol=6.4×10-3g
煤样中硫的质量分数=$\frac{m(S)}{m(样品)}$=$\frac{6.4×1{0}^{-3}g}{1g}$=0.64%;
答:煤样中硫的质量分数为0.64%.
点评 本题考查方程式的计算,注意元素守恒法的计算及应用,题目难度不大.

练习册系列答案
相关题目
13.下列各溶液中加入少量Na2O2,不会出现浑浊的是( )
| A. | 饱和NaHCO3溶液 | B. | 饱和Ca(HCO3)溶液 | C. | CuSO4稀溶液 | D. | FeCl2溶液 |
7.NA为阿伏加德罗常效,下列叙述错误的是( )
| A. | 18g H2O中含有的质子数为10NA | |
| B. | 1L0.1mol/LAl2(SO4)3溶液中,Al3+的数目为0.2NA | |
| C. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
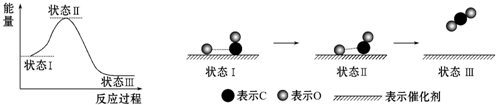
14.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下:
下列说法中正确的是( )

下列说法中正确的是( )
| A. | CO和O生成CO2是吸热反应 | B. | 状态Ⅰ→状态Ⅲ表示CO和O反应的过程 | ||
| C. | CO和O生成了具有非极性键的CO2 | D. | 在该过程中,CO断键形成C和O |
5.五种短周期元素在周期表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请回答下列问题:
(1)请写出元素名称:X碳Y氮W氯;
(2)元素Z位于周期表中第三周期ⅢA族;
(3)写出X单质与Y的最高价氧化物水化物浓溶液在受热时反应的化学方程式C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O;M的最高价氧化物的水化物化学式为HClO4.
| X | Y | ||
| Z | W | M |
(1)请写出元素名称:X碳Y氮W氯;
(2)元素Z位于周期表中第三周期ⅢA族;
(3)写出X单质与Y的最高价氧化物水化物浓溶液在受热时反应的化学方程式C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O;M的最高价氧化物的水化物化学式为HClO4.
6.【物质结构与性质】.
X、Y、Z、W、J是元素周期表前四周期中的五种常见元素.其相关信息如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是146C;
(2)元素Y位于元素周期表第三周期第VIA族;
(3)元素Z的原子最外层共有7种不同运动状态的电子;基态Z原子中,电子占有的最高能层符号为3p;
(4)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1,W的基态原子核外价电子排布图是 ;
;
(5)元素Y与元素Z相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是bce;
a.常温下,Y的单质与Z的单质状态不同
b.Z的电负性大于Y
c.Z的氢化物比Y的氢化物稳定
d.在反应中,Y原子得电子数比Z原子得电子数多
e.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
(6)J的元素名称氮,在周期表中位于p区.写出J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐的离子方程式NH3+H+=NH4+.
X、Y、Z、W、J是元素周期表前四周期中的五种常见元素.其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
| J | J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐 |
(2)元素Y位于元素周期表第三周期第VIA族;
(3)元素Z的原子最外层共有7种不同运动状态的电子;基态Z原子中,电子占有的最高能层符号为3p;
(4)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1,W的基态原子核外价电子排布图是
 ;
;(5)元素Y与元素Z相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是bce;
a.常温下,Y的单质与Z的单质状态不同
b.Z的电负性大于Y
c.Z的氢化物比Y的氢化物稳定
d.在反应中,Y原子得电子数比Z原子得电子数多
e.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
(6)J的元素名称氮,在周期表中位于p区.写出J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐的离子方程式NH3+H+=NH4+.