题目内容
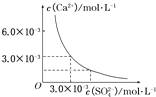
已知25℃时,CaSO4在水中的沉淀溶解平衡曲线,如图所示,向100mL该条件下的CaSO4饱和溶液中,加入400mL 0.01mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是( )
A.溶液中析出CaSO4沉淀,最终溶液中c(SO
| ||
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO
| ||
C.溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO
| ||
D.溶液中无沉淀析出,但最终溶液中c(SO
|

由图示可知,在该条件下,CaSO4饱和溶液中,c(Ca2+)=c( SO42-)=3.0×10-3 mol/L,Ksp(CaSO4)=9.0×10-6.当向100 mL该条件下的CaSO4饱和溶液中加入400 mL 0.01 mol/L的Na2SO4溶液后,混合液中c(Ca2+)=
=6.0×10-4 mol/L,c(SO42-)=
=8.6×10-3 mol/L,溶液中c(Ca2+)?c( SO42- )=5.16×10-6<Ksp(CaSO4)=9.0×10-6,所以混合液中无沉淀析出,最终溶液中硫酸根离子浓度增大;
故选D.
| 0.1L×3.0×10-3mol/L |
| 0.1L+0.4L |
| 0.1L×3.0×10-3mol/L+0.4L×0.01mol/L |
| 0.1L+0.4L |
故选D.

练习册系列答案
相关题目
已知25℃时,CaSO4在水中沉淀溶解平衡曲线如图所示,向100 mL该条件下的CaSO4饱和溶液中,加入400 mL 0.01 mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是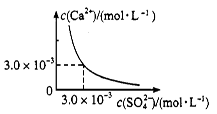
| A.溶液中无沉淀析出,但最终溶液中c(SO42-)较原来大 |
| B.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)较原来大 |
| C.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小 |
| D.溶液中析出CaSO4固体沉淀,溶液中c(Ca2+)、c(SO42-)都变小 |
 已知25℃时,CaSO4在水中的沉淀溶解平衡曲线,如图所示,向100mL该条件下的CaSO4饱和溶液中,加入400mL 0.01mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是( )
已知25℃时,CaSO4在水中的沉淀溶解平衡曲线,如图所示,向100mL该条件下的CaSO4饱和溶液中,加入400mL 0.01mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是( )
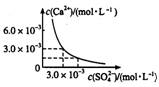

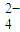 )较原来大
)较原来大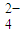 )都变小
)都变小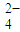 )都变小
)都变小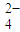 )较原来大
)较原来大