题目内容
下列物质,按熔点由低到高的顺序排列的是( )
①SiO2、NaCl、Na、CH4;
②NaCl、Na、H2O、CH4;
③F2、Cl2、Br2、I2;
④H2、Na、NaCl、Si.
①SiO2、NaCl、Na、CH4;
②NaCl、Na、H2O、CH4;
③F2、Cl2、Br2、I2;
④H2、Na、NaCl、Si.
| A、①③ | B、②④ | C、①② | D、③④ |
考点:晶体熔沸点的比较
专题:
分析:一般来说,晶体熔沸点高低顺序是:原子晶体>离子晶体>分子晶体;分子晶体中,分子晶体的熔沸点与其相对分子质量成正比,但含有氢键的熔沸点较高,据此分析解答.
解答:
解:一般来说,晶体熔沸点高低顺序是:原子晶体>离子晶体>分子晶体;分子晶体中,分子晶体的熔沸点与其相对分子质量成正比,但含有氢键的熔沸点较高,
①SiO2是原子晶体、NaCl是离子晶体、Na是金属晶体、CH4分子晶体,熔沸点从低到高顺序是,故CH4、Na、NaCl、SiO2,故错误;
②NaCl是离子晶体、Na是金属晶体、H2O和CH4是分子晶体,但水中含有氢键,钠的熔沸点低于水,所以熔沸点从低到高顺序是CH4、Na、H2O、NaCl,故错误;
③F2、Cl2、Br2、I2都是分子晶体,其相对分子质量随着原子序数增大而增大,所以其熔沸点随着原子序数增大而增大,则熔沸点从低到高顺序是F2、Cl2、Br2、I2,故正确;
④H2是分子晶体、Na是金属晶体、NaCl是离子晶体、Si是原子晶体,熔沸点从低到高顺序是H2、Na、NaCl、Si,故正确;
故选D.
①SiO2是原子晶体、NaCl是离子晶体、Na是金属晶体、CH4分子晶体,熔沸点从低到高顺序是,故CH4、Na、NaCl、SiO2,故错误;
②NaCl是离子晶体、Na是金属晶体、H2O和CH4是分子晶体,但水中含有氢键,钠的熔沸点低于水,所以熔沸点从低到高顺序是CH4、Na、H2O、NaCl,故错误;
③F2、Cl2、Br2、I2都是分子晶体,其相对分子质量随着原子序数增大而增大,所以其熔沸点随着原子序数增大而增大,则熔沸点从低到高顺序是F2、Cl2、Br2、I2,故正确;
④H2是分子晶体、Na是金属晶体、NaCl是离子晶体、Si是原子晶体,熔沸点从低到高顺序是H2、Na、NaCl、Si,故正确;
故选D.
点评:本题考查晶体熔沸点高低判断,明确晶体类型与熔沸点的关系是解本题关键,注意氢键对分子晶体熔沸点的影响,注意钠的熔沸点较低,为易错点.

练习册系列答案
相关题目
下列物质中溶于水中后能生成两种酸的是( )
| A、HCl |
| B、CO2 |
| C、SO2 |
| D、Cl2 |
合成氨工业对国民经济和社会发展具有重要的意义.其原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,从化学平衡角度考虑,为了提高氨气的产率,可以选择的方法是( )①升高温度 ②增大压强 ③使用催化剂 ④及时分离出NH3.
| A、①③ | B、①② | C、②③ | D、②④ |
在8NH3+3Cl2═6NH4Cl+N2反应中,若有2mol N2生成,发生氧化反应的物质的量是( )
| A、16 mol NH3 |
| B、8 mol NH3 |
| C、4 mol NH3 |
| D、3 mol NH3 |
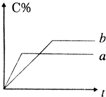 可逆反应A(s)+B(g)?n C (g)△H=Q (n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示.下列有关叙述中一定正确的是( )
可逆反应A(s)+B(g)?n C (g)△H=Q (n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示.下列有关叙述中一定正确的是( )| A、其他条件相同,a表示使用了催化剂,b没有使用催化剂 |
| B、其他条件相同,若只改变压强,则a比b的压强大且n≥2 |
| C、其他条件相同,若只改变温度,则a比b的温度高且Q>0 |
| D、其他条件相同,a表示减少A的物质的量 |
已知:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206kJ?mol-1CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247kJ?mol-1
C-H键的键能约为413kJ/mol,O-H键的键能约为463kJ/mol,H-H键的键能约为436kJ/mol,则CO2中C=O键的键能约为( )
C-H键的键能约为413kJ/mol,O-H键的键能约为463kJ/mol,H-H键的键能约为436kJ/mol,则CO2中C=O键的键能约为( )
| A、797.5kJ/mol |
| B、900.5kJ/mol |
| C、962.5kJ/mol |
| D、1595kJ/mol |
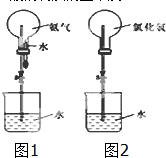 某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).
某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).