题目内容
下列事实能说明Al的金属活动性比Cu强的是( )
| A、常温下将铝和铜用导线连接组成原电池放入到氢氧化钠溶液中 |
| B、常温下将铝和铜用导线连接组成原电池放入到稀盐酸溶液中 |
| C、与氯气反应时,铝失去3个电子,而铜失去2个电子 |
| D、常温下,铝在浓硝酸中钝化而铜不发生钝化 |
考点:常见金属的活动性顺序及其应用
专题:元素及其化合物
分析:根据金属活动性顺序回答,铁比铜活泼,反应中易失去电子,能把铜从其盐溶液中置换出来,形成原电池反应时,活泼金属为负极,以此解答.
解答:
解:A、铝和铜用导线连接组成原电池放入到氢氧化钠溶液中,自发的氧化还原反应发生在金属铝和氢氧化钠之间,铜和氢氧化钠不反应,金属铝是负极,是金属本身性质决定的,不能说明Al的金属活动性比Cu强,故A错误;
B、铝和铜用导线连接放入到稀盐酸溶液中形成原电池反应时,活泼金属铝为负极,能说明Al的金属活动性比Cu强,故B正确;
C、不能根据失电子的多少来确定金属的活泼性强弱,可以根据失电子的能力来判断,故C错误;
D、常温下,铝在浓硝酸中钝化而铜不发生钝化,是由物质本身的性质决定的,不能说明Al的金属活动性比Cu强,故D错误;
故选B.
B、铝和铜用导线连接放入到稀盐酸溶液中形成原电池反应时,活泼金属铝为负极,能说明Al的金属活动性比Cu强,故B正确;
C、不能根据失电子的多少来确定金属的活泼性强弱,可以根据失电子的能力来判断,故C错误;
D、常温下,铝在浓硝酸中钝化而铜不发生钝化,是由物质本身的性质决定的,不能说明Al的金属活动性比Cu强,故D错误;
故选B.
点评:本题考查金属的活泼性的比较,侧重于学生的分析能力的考查,为高频考点,注意把握金属活泼性比较的角度,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4LCC14中含有的分子数目为NA |
| B、25℃时,1 L pH=1的醋酸溶液中含有醋酸分子数大于0.1 NA |
| C、含0.1 mol FeCl3的饱和溶液中Fe3+数目为0.1 NA |
| D、常温常压下,0.1mo1C12溶于足量NaOH溶液中,转移的电子数目为0.2NA |
下列各组物质的晶体中,化学键类型和晶体类型都相同的是( )
| A、CO2和CH4 |
| B、KOH和CH4 |
| C、SiO2和CO2 |
| D、Na和HCl |
实验中剩余的药品应( )
| A、放回原瓶 |
| B、拿出实验室 |
| C、放入垃圾筒 |
| D、放入指定容器 |
下列微粒中,原子半径依次增大的是( )
| A、Mg、Ca、Ba |
| B、I、Br、Cl |
| C、O、Na、S |
| D、Al、Si、P |
利用反应:2NO(g)+2CO(g)?2C02(g)+N2(g)△H=-746.8kJ?mol-1,可净化汽车尾气,如果要同时提高反应的速率和N0的转化率,采取的措施是( )
| A、降低温度 |
| B、增大压强 |
| C、升高温度同时充入N2 |
| D、及时将C02和N2从反应体系中移走 |
元素A的原子最外层有7个电子,元素B的原子最外层有2个电子,则A与B形成的化合物可能的化学式是( )
| A、B2A3 |
| B、B2A |
| C、BA2 |
| D、BA |
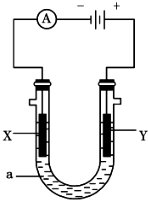 (1)电解池中与外电源负极相连的电极反应式为
(1)电解池中与外电源负极相连的电极反应式为