题目内容
16.KMnO4能将草酸(H2C2O4)氧化.在25℃下,某同学欲通过对比实验探究初始pH和草酸浓度对该反应速率的影响.完成实验设计表,表中不要留空格. | 初始pH | V(KMnO4)/mL | V(H2C2O4)/mL | V(H2O)/mL |
| ① | 4 | 20 | 10 | |
| ② | 5 | 10 | 5 | |
| ③ | 20 | 10 |
步骤Ⅰ称取2.50g碳酸钙试样,溶解于稀盐酸,以CaC2O4形式沉淀钙.
沉淀Ⅱ将沉淀过滤洗涤,溶于稀硫酸后定容在250mL容量瓶中.
步骤Ⅲ每次取20.00mL溶液,用0.020mol/L KMnO4标准溶液滴定,三次滴定消耗标准液的平均体积为36.42mL.
①滴定过程中用到的玻璃仪器有酸式滴定管、锥形瓶,滴定终点的现象是加入最后一滴KMnO4溶液,溶液变为浅红色,浅红色30s内不褪去,说明滴定到终点.
②步骤Ⅱ中若将沉淀溶于稀盐酸,会使测定结果偏高(填“偏高”“偏低”或“无影响”).
③试样中钙的质量分数是91.05%.
分析 (1)该实验探究不同的初始pH和草酸溶液浓度对反应速率的影响,所以KMnO4的浓度不变,探究外界条件对反应速率的影响,需保证其他条件相同时来做实验;
(2)①KMnO4标准溶液用带玻璃活塞的酸式滴定管,待测液用锥形瓶盛放;利用高锰酸钾本身颜色判断滴定到终点;
草酸与高锰酸钾反应是锰离子和二氧化碳、水;
②盐酸会与酸性高锰酸钾反应,导致高锰酸钾消耗更多;
③根据关系式2KMnO4~5H2C2O4计算出草酸的物质的量,再根据关系式H2C2O4~CaC2O4~CaCO3计算碳酸钙的物质的量,最后得出质量分数.
解答 解:(1)该实验探究不同的初始pH和草酸溶液浓度对反应速率的影响,实验要求控制KMnO4溶液初始浓度相同,则KMnO4溶液的体积为20mL,根据实验②可知总体积为35mL,每次实验总体积都是35mL,则实验①加水的体积应为5mL,实验③加入草酸的体积应是5mL,实验①与实验②溶液PH不同,其他条件相同,则探究不同的初始pH对反应速率的影响,实验③与实验②探究草酸溶液浓度对反应速率的影响,所以溶液PH相同,应为5,
故答案为:
 | 初始pH | V(KMnO4)/mL | V(H2C2O4)/mL | V(H2O)/mL |
| ① | 5 | |||
| ② | 20 | |||
| ③ | 5 | 5 |
(2)①KMnO4标准溶液有强氧化性,会腐蚀橡胶,用带玻璃活塞的酸式滴定管,待测液用锥形瓶盛放;高锰酸钾本身有颜色,故不需要另加指示剂,草酸反应完毕,加入最后一滴KMnO4溶液,溶液变为浅红色,浅红色30s内不褪去,说明滴定到终点,
故答案为:酸式滴定管、锥形瓶;加入最后一滴KMnO4溶液,溶液变为浅红色,浅红色30s内不褪去,说明滴定到终点;
②盐酸会与酸性高锰酸钾反应,导致高锰酸钾消耗更多,实验是通过高锰酸钾的量算出样品中钙的含量,所以用盐酸会使结果偏高,
故答案为:偏高;
③草酸与高锰酸钾反应生成锰离子、二氧化碳和水,其反应的离子方程式为:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O,
根据关系式2KMnO4~~~~~~~~~~~~5H2C2O4
2 5
0.020mol/L×36.42×10-3L n(H2C2O4)
n(H2C2O4)=$\frac{0.020mol/L×36.42×1{0}^{-3}L×5}{2}$,
则250mL容量瓶中草酸物质的量为:$\frac{0.020mol/L×36.42×1{0}^{-3}L×5}{2}$×$\frac{250mL}{20mL}$,
再根据关系式H2C2O4~CaC2O4~CaCO3可知碳酸钙的物质的量与草酸物质的量相等,
则碳酸钙的质量分数为:$\frac{碳酸钙的质量}{样品总质量}×100%$=$\frac{0.020mol/L×36.42×1{0}^{-3}L×5}{2}$×$\frac{250mL}{20mL}$×100g/mol÷2.50g×100%=91.05%,
故答案为:91.05%.
点评 本题考查了定量实验探究,是高考热点,涉及影响化学反应速率的因素和利用氧化还原滴定测定物质的含量,题目综合性强,注意在探究外界条件对反应速率的影响时控制变量法的使用,定量计算时注意实验过程中只是取了样品的一部分,容易忽略.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
6.将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)═NH3(g)+HI(g);②2HI(g)═H2(g)+I2(g)达到平衡时,c(H2)=0.5mol•L-1,c(HI)=5mol•L-1,则此温度下反应①的平衡常数为
( )
( )
| A. | 36 | B. | 30 | C. | 25 | D. | 20 |
4.已知3.01×1023个X气体分子的质量为16g,则X气体的相对分子质量是( )
| A. | 8g•mol-1 | B. | 16 g•mol-1 | C. | 32 | D. | 64 g•mol-1 |
11.KI+5KIO3+3H2S=3I2+3K2SO4+3H2O,下列说法正确的是( )
| A. | 3 mol H2S可还原4mol的KIO3 | |
| B. | 氧化剂和还原剂物质的量之比为5:4 | |
| C. | I2是还原产物,K2SO4是氧化产物 | |
| D. | 1molKIO3可氧化0.2mol的KI |
1.类比法是化学学习过程中一种重要方法,以下类比关系正确的是( )
| A. | 工业上可以电解熔融的氯化镁或氯化铝制得相应的金属单质 | |
| B. | Cl2、Br2、I2都具有强氧化性,都能将铁氧化成+3价的铁盐 | |
| C. | 二氧化碳和二氧化硫都是氧化物,两者都不能和氯化钙溶液反应 | |
| D. | 氧化铁和氧化亚铁都是碱性氧化物,和硝酸反应都只生成盐和水 |
8.等体积、等浓度的下列溶液,含Cl-最少的溶液是( )
| A. | CaCl2 | B. | KCl | C. | AlCl3 | D. | SnCl4 |
8.乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味.实验室制备乙酸异戊酯的反应、装置示意图(如图1)和有关数据如下: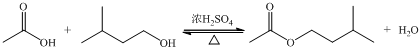
实验步骤:
在A中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是:球形冷凝管
(2)在洗涤、分液操作中,应充分振荡,然后静置,待分层后b(填标号).
a.直接将乙酸异戊酯从分液漏斗上口倒出
b.直接将乙酸异戊酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(3)本实验中加入过量乙酸的目的是:提高醇的转化率.
(4)实验中加入少量无水MgSO4的目的是:干燥.
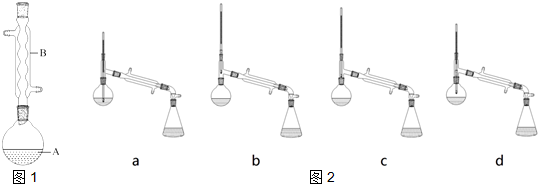
(5)如图2,在蒸馏操作中,仪器选择及安装都正确的是:b (填标号).
(6)本实验的产率是:d(填标号).
a.30% b.40% c.50% d.60%
(7)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”).

| 相对分子质量 | 密度/(g?cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
在A中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是:球形冷凝管
(2)在洗涤、分液操作中,应充分振荡,然后静置,待分层后b(填标号).
a.直接将乙酸异戊酯从分液漏斗上口倒出
b.直接将乙酸异戊酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(3)本实验中加入过量乙酸的目的是:提高醇的转化率.
(4)实验中加入少量无水MgSO4的目的是:干燥.
(5)如图2,在蒸馏操作中,仪器选择及安装都正确的是:b (填标号).

(6)本实验的产率是:d(填标号).
a.30% b.40% c.50% d.60%
(7)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”).
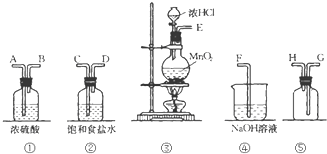 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图:
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图: