题目内容
下列热化学方程式中的△H能表示物质燃烧热的是( )
| A、2CO(g)+O2(g)═2CO2(g);△H=-556kJ?mol-1 | ||
| B、CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890kJ?mol-1 | ||
C、H2(g)+
| ||
| D、H2(g)+Cl2(g)═2HCl(g);△H=-184.6kJ?mol-1 |
考点:燃烧热
专题:化学反应中的能量变化
分析:燃烧热表示1mol可燃物完全燃烧生成稳定氧化物所放出的热量,表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物.
解答:
解:A.CO的化学计量数为2,所以△H不代表燃烧热,故A错误;
B.CH4的化学计量数为1,产物为稳定氧化物,符合燃烧热的定义,所以△H代表燃烧热,故B正确;
C.H2O为气态不是最稳定的氧化为,所以△H不代表燃烧热,故C错误;
D.燃烧热表示1mol可燃物完全燃烧生成稳定氧化物放出的热量,HCl不是氧化物,故不符合燃烧热的定义,故D错误;
故选:B.
B.CH4的化学计量数为1,产物为稳定氧化物,符合燃烧热的定义,所以△H代表燃烧热,故B正确;
C.H2O为气态不是最稳定的氧化为,所以△H不代表燃烧热,故C错误;
D.燃烧热表示1mol可燃物完全燃烧生成稳定氧化物放出的热量,HCl不是氧化物,故不符合燃烧热的定义,故D错误;
故选:B.
点评:本题考查了燃烧热的概念,题目难度不大,理解此概念是应注意:可燃物的物质的量必须是1mol;生成的产物必须是稳定氧化物,例如碳形成二氧化碳、氢形成液态水.

练习册系列答案
相关题目
下列关于油脂的叙述不正确的是 (?)
| A、油脂属于酯类 |
| B、天然油脂没有固定的熔、沸点 |
| C、是高级脂肪酸的甘油酯 |
| D、油脂都不能使溴水退色 |
已知反应:①2C(s)+O2(g)=2CO(g);△H=-221kJ/mol②H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol(稀溶液);下列结论正确的是( )
| A、碳的燃烧热为110.5 kJ/mol |
| B、1mol碳充分燃烧放出的热量大于110.5kJ |
| C、浓硫酸与稀NaOH溶液反应生成1 mol水,放出的热量为57.3 kJ |
| D、稀醋酸与稀NaOH溶液反应生成1 mol水,放出的热量为57.3 kJ |
有关氨气的实验较多,下面对这些实验的实验原理的分析中,正确的是( )
| A、氨气极易溶解于水的性质可以解释氨气的喷泉实验 |
| B、氨气的还原性可以解释氨气与氯化氢的反应 |
| C、铵盐的水溶性大是实验室中用NH4Cl和Ca(OH)2的混合物制取氨气的原因 |
| D、实验室可以用浓硫酸来干燥氨气 |
某浓度的硝酸与过量铁粉反应时生成了4.48LN2O气体(标准状况下),若改与铝反应(生成NO气体),则最后可溶解的铝的质量是( )
| A、13.5g | B、9g |
| C、27g | D、8.9g |
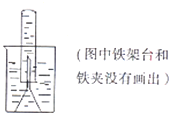 某同学取一张铝箔,并用针刺一些小孔,然后取一药匙过氧化钠粉末,用铝箔包好,放入如图所示装置倒扣的漏斗中.
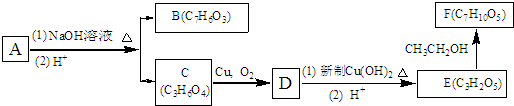
某同学取一张铝箔,并用针刺一些小孔,然后取一药匙过氧化钠粉末,用铝箔包好,放入如图所示装置倒扣的漏斗中.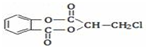 )在一定条件下可以发生如图所示的转化(其它产物和水已略去).请回答下列问题:
)在一定条件下可以发生如图所示的转化(其它产物和水已略去).请回答下列问题: