题目内容
将一定量的NaHCO3和Na2O2混合,在密闭容器中充分混合加热后,最后排出气体,得残留固体40.8 g,残留固体恰好与1 L 1 mol/L的稀盐酸溶液完全反应,下列说法正确的是( )
A.40.8 g固体物质为Na2CO3
B.40.8 g固体物质为NaOH和Na2O2混合物
C.40.8 g固体物质为0.2 mol NaOH和0.4 mol Na2CO3混合物
D.40.8 g固体物质为0.2 mol NaOH、0.2 mol Na2CO3、0.2 mol Na2O2混合物
D
【解析】
试题分析:A.若40.8 g固体物质为Na2CO3,则其物质的量是n(Na2CO3)= 40.8 g÷106g/mol=0.385mol,与盐酸反应时消耗盐酸的物质的量是0.385mol×2=0.77mol,与题干中消耗1mol的盐酸不符合,错误;B.NaHCO3受热分解产生的固体物质中应该含有Na2CO3,所以根据元素守恒,40.8 g固体物质不可能为NaOH和Na2O2混合物,错误;C. 0.2 mol NaOH和0.4 mol Na2CO3混合物的质量是0.2 mol× 40g/mol +0.4 mol ×106g/mol=50.8 g,质量不符合,错误;D 0.1 mol NaOH、0.2 mol Na2CO3、0.2 mol Na2O2混合物的质量是0.1 mol×40g/mol+0.2 mol×106g/mol+0.2 mol×78g/mol =40.8 g,其中含有的Na元素的物质的量是0.2mol+0.2mol×2+0.2mol×2=1mol,所以根据元素守恒,加入HCl时完全反应产生NaCl消耗的HCl的物质的量是1mol,与题干吻合,正确。
考点:考查钠的化合物的性质及混合物成分的确定的知识。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案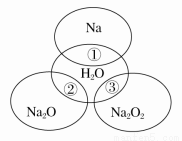
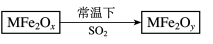 则下列判断正确的是( )
则下列判断正确的是( )