题目内容
(10分)常温常压下,断裂1mol气体分子化学键所吸收的能量或形成1mol气体分子化学键所放出的能量称为键能(单位为kJ.mol-1),根据下表键能数据(kJ·mol-1)回答问题:
化学键 | C-F | C-Cl | C-I | H-H | S=S | H-S |
键能 | 427 | 330 | 218 | 436 | 255 | 339 |
(1)由表中数据预测C-Br键的键能范围:_________<C-Br键能<_________(回答数值和单位)
(2)热化学方程式2H2(g)+S2(g) = 2H2S(g);△H= QkJ·mol-1;则Q=
(3)已知下列热化学方程式:
①O2 (g) = O+2(g) + e- 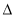 H1= +1175.7 kJ·mol-1 ②PtF6(g) + e- = PtF6—(g)
H1= +1175.7 kJ·mol-1 ②PtF6(g) + e- = PtF6—(g) 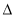 H2= -771.1 kJ·mol-1
H2= -771.1 kJ·mol-1
③O2+PtF6-(s) = O2+(g) + PtF6-(g)  H3= +482.2 kJ·mol-1
H3= +482.2 kJ·mol-1
则反应O2(g) + (g) = O2+PtF6-(s) 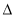 H=_____________ kJ·mol-1。
H=_____________ kJ·mol-1。
(10分) (1)218 KJ·mol-1 330 KJ·mol-1 (2)—229 (3)PtF6 ;—77.6
【解析】
试题分析:(1)由于Br元的原子半径大于Cl,小于I原子,所以由表中数据预测C-Br键的键能范围应该是小于3307KJ/mol,大于218KJ/mol,(2)热化学方程式2H2(g)+S2(g) = 2H2S(g);△H= QkJ·mol-1;则该反应的反应热是断裂2mol的H—H和1mol的S—S所吸收的热量与形成4mol的H—S所释放的热量的差,Q=[(2×436+1×255)—4×339] KJ/mol =—229KJ/mol;①+②—③,整理可得:O2(g) + PtF6(g) = O2+PtF6-(s) ΔH=—77.6 KJ/mol。
考点:考查反应热与键能的关系、热化学方程式的书写及盖斯定律的应用的知识。

 阅读快车系列答案
阅读快车系列答案 pC(g) + qD(g) △H<0,下列说法不正确的是
pC(g) + qD(g) △H<0,下列说法不正确的是