题目内容
13.38.4克铜跟适量的浓硝酸反应,铜全部作用后共收集到气体22.4升(标准状况),反应消耗的HNO3的物质的量可能是( )| A. | 1.0摩尔 | B. | 1.6摩尔 | C. | 2.2摩尔 | D. | 2.0摩尔 |
分析 铜和硝酸反应,随着浓度的减少,硝酸的还原产物的价态越低,铜和浓硝酸反应生成NO2,而与稀硝酸反应时则生成NO,故生成的气体有NO2和NO,根据混合气体的物质的量可得被还原的硝酸的物质的量,根据生成硝酸铜的物质的量可知表现酸性的硝酸的物质的量,以此计算反应消耗的硝酸的物质的量.
解答 解:铜和硝酸反应,随着浓度的减少,硝酸的还原产物的价态越低,铜和浓硝酸反应生成NO2,而与稀硝酸反应时则生成NO,故生成的气体有NO2和NO,
则n(NO2)+n(NO)=$\frac{22.4L}{22.4L/mol}$=1.0mol,
即被还原的硝酸的物质的量为1.0mol,
n(Cu)=$\frac{38.4g}{64g/mol}$=0.6mol,则生成n(Cu(NO3)2)=0.6mol,
可知表现酸性的硝酸的物质的量为0.6mol×2=1.2mol,
则:参加反应的硝酸的物质的量为:1.0mol+1.2mol=2.2mol,
故选C.
点评 本题考查化学方程式的计算,题目难度中等,侧重于学生的分析、计算能力的考查,但该题可不书写写有关反应的方程式,注意浓硝酸和稀硝酸的性质的不同,从质量守恒的角度解答该题.

练习册系列答案
相关题目
1.下列存在顺反异构的有机物是( )
| A. | CH3CH=CH2 | B. | Br2C=CHCH2COOH | C. | 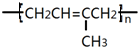 | D. | 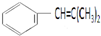 |
18.元素的性质呈现周期性变化的根本原因是( )
| A. | 原子半径呈周期性变化 | |
| B. | 元素的化合价呈周期性变化 | |
| C. | 元素的金属性和非金属性呈周期性变化 | |
| D. | 元素原子的核外电子排布呈周期性变化 |
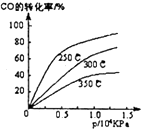 工业合成甲醇反应如下:CO(g)+2H2(g)?CH3OH(g);△H请回答下列问题:
工业合成甲醇反应如下:CO(g)+2H2(g)?CH3OH(g);△H请回答下列问题: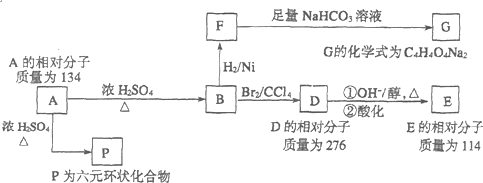
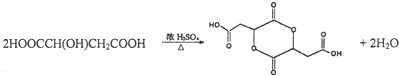 .
.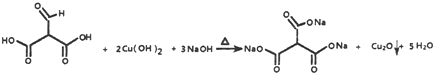 .
.
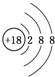 .元素K名称为氯在周期表中的位置第三周期第ⅦA族.
.元素K名称为氯在周期表中的位置第三周期第ⅦA族.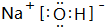
 HClO+HCl.
HClO+HCl.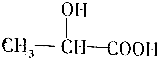 ,
,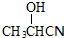 .
.