题目内容
3.下列分子晶体中,关于熔、沸点高低的叙述正确的是( )| A. | H2>N2>O2 | |
| B. | NH3>AsH3>PH3 | |
| C. | Cl2>Br2>I2 | |
| D. | C(CH3)4>(CH3)2CHCH2CH3>CH3CH2CH2CH2CH3 |
分析 组成和结构相似的分子晶体,一般来说相对分子质量越大,分子间作用力越强,熔沸点越高.例如:I2>Br2>Cl2>F2.
组成和结构相似的分子晶体,如果分子之间存在氢键,则分子之间作用力增大,熔沸点出现反常.有氢键的熔沸点较高.例如,熔点:HI>HBr>HF>HCl;沸点:HF>HI>HBr>HCl.同类有机物,支链越多,沸点越低.
解答 解:A.组成和结构相似的分子晶体,一般来说相对分子质量越大,分子间作用力越强,熔沸点越高,所以O2>N2>H2,故A错误;
B.NH3存在氢键,熔沸点高于AsH3,AsH3、PH3无氢键,相对分子质量越大,熔沸点越高,所以熔、沸点NH3>AsH3>PH3,故B正确;
C.Cl2、Br2、I2无氢键,相对分子质量越大,熔沸点越高,所以熔、沸点I2>Br2>Cl2,故C错误;
D.同类有机物,支链越多,沸点越低,所以熔、沸点CH3CH2CH2CH2CH3>(CH3)2CHCH2CH3>C(CH3)4,故D错误;
故选B.
点评 本题考查分子晶体熔沸点高低的比较,题目难度不大,注意同种晶体熔沸点高低比较的方法和角度,注意氢键对分子晶体溶沸点的影响,注意同类有机物,支链越多,沸点越低.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.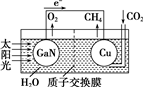 科学家用氮化镓材料与铜组装成如图的人工光合系统,实现了以CO2和H2O为原料合成CH4.下列有关说法中正确的是( )
科学家用氮化镓材料与铜组装成如图的人工光合系统,实现了以CO2和H2O为原料合成CH4.下列有关说法中正确的是( )
 科学家用氮化镓材料与铜组装成如图的人工光合系统,实现了以CO2和H2O为原料合成CH4.下列有关说法中正确的是( )
科学家用氮化镓材料与铜组装成如图的人工光合系统,实现了以CO2和H2O为原料合成CH4.下列有关说法中正确的是( )| A. | 该装置是将化学能转化为电能 | |
| B. | 氮化镓电极是阳极 | |
| C. | 铜电极表面的电极反应式为CO2+8e-+8H+═CH4+2H2O | |
| D. | 可用盐酸作该装置的电解液 |
8.下列各组物质熔化或升华时,所克服的粒子间作用属于同种类型的是( )
| A. | 碘和干冰升华 | B. | 镁和硫熔化 | ||
| C. | 氯化钠和蔗糖熔化 | D. | Na2O和SiO2熔化 |
15.有8种物质:①甲烷;②苯;③聚乙烯;④聚1,3-丁二烯;⑤2-丁炔;⑥环己烷;⑦邻二甲苯;⑧环己烯.既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ③④⑤⑧ | B. | ④⑤⑧ | C. | ④⑤⑦⑧ | D. | ③④⑤⑦⑧ |
12.下列关于化学反应的描述中正确的是( )
| A. | 当一个化学反应在一定条件下达到最大限度时,反应速率也最大 | |
| B. | 用一定量的锌片和足量的稀硫酸反应制氢气时,加入少量氧化铜,可以加快反应的速率且生成氢气的总量不变 | |
| C. | 燃烧一定是放热反应,也是氧化还原反应 | |
| D. | 化学反应中能量变化的大小与反应物的状态无关 |
13.下列装置能构成原电池的是( )
| A. | 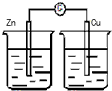 稀H2SO4 | B. | 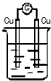 AgNO3 | C. | 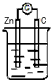 甘油 | D. | 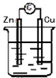 稀H2SO4 |
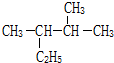 的系统命名为2,3-二甲基戊烷.
的系统命名为2,3-二甲基戊烷.