题目内容
7.电解饱和食盐水可以得氯气,氢气和氢氧化钠.当标准状况下,收集到H22.24L时,(1)参加反应的氯化钠的质量是11.7g
(2)可生成氢氧化钠的质量是8g
(3)理论上可收集到标况下Cl22.24L(忽略Cl2在水中的溶解)
分析 电解饱和食盐水时反应方程式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,n(H2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,
(1)根据方程式知n(NaCl)=2n(H2),m(NaCl)=nM;
(2)据Na原子守恒得生成n(NaOH)=n(NaCl),m(NaOH)=nM;
(3)根据方程式知,n(H2)=n(Cl2),V=nVm.
解答 解:电解饱和食盐水时反应方程式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,n(H2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,
(1)根据方程式知n(NaCl)=2n(H2)=2×0.1mol=0.2mol,m(NaCl)=0.2mol×58.5g/mol=11.7g,
故答案为:11.7;
(2)根据Na原子守恒得生成n(NaOH)=n(NaCl)=0.2mol,m(NaOH)=0.2mol×40g/mol=8g,
故答案为:8;
(3)根据方程式知,n(H2)=n(Cl2)=0.1mol,V=nVm=0.1mol×22.4L/mol=2.24L,
故答案为:2.24.
点评 本题考查化学方程式有关计算,为高频考点,明确各个物理量之间的关系式是解本题关键,侧重考查学生计算能力,会正确运用原子守恒及关系式,题目难度不大.

练习册系列答案
相关题目
18.下列固体加热熔化时需破坏非极性共价键的是( )
| A. | 碘单质 | B. | 金刚石 | C. | 二氧化硅 | D. | 氢氧化钠 |
15.有4.8g CuO、Fe2O3混合物与充足的CO于加热条件充分反应,反应后全部气体用0.6mol/L Ba(OH)2溶液100mL处理,有白色沉淀生成.又知反应后生成的气体质量为3.52g,下列有关叙述中正确的是( )
| A. | 原混合物中CuO与Fe2O3的质量比为2:1 | |
| B. | 生成的CO2已被Ba(OH)2溶液完全吸收,Ba2+沉淀完全 | |
| C. | 在吸收CO2后的溶液中有Ba(HCO3)2 | |
| D. | 原混合物中CuO与Fe2O3物质的量的比为l:l |
2.在一定温度和压强下40mL的XY2气体和20mL的Y2气体化合成40mL的Z气体,则Z气体的分子式表示为( )
| A. | X2Y4 | B. | XY3 | C. | X2Y6 | D. | X3Y |
17.下列可被工业上采用的冶金方法是( )
| A. | 电解熔融的氯化铝制铝 | B. | 电解熔融的氯化镁制镁 | ||
| C. | 电解氯化钠溶液制钠 | D. | 高温下用H2还原氧化镁制镁 |
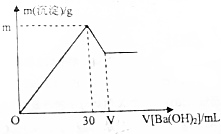 现有10mL1mol/LAl2(SO4)3溶液,向其中逐滴滴加一定物质的量浓度的Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.(已知:Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O)
现有10mL1mol/LAl2(SO4)3溶液,向其中逐滴滴加一定物质的量浓度的Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.(已知:Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O)

 .
.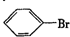 .
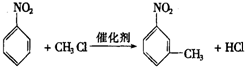
.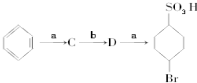 ”中的反应中属于取代反应的是ab,属于加成反应的是c(填字母).
”中的反应中属于取代反应的是ab,属于加成反应的是c(填字母).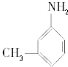 的所有原子不是(填“是”或“不是”)在同一平面上.
的所有原子不是(填“是”或“不是”)在同一平面上.