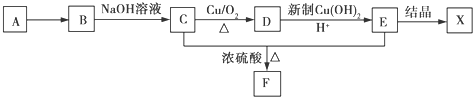
题目内容
水溶液中能大量共存的一组离子是( )
| A、K+、H+、I-、ClO- |
| B、Na+、Fe3+、SO42-、OH- |
| C、Al3+、NH4+、AlO2-、NO3- |
| D、Mg2+、Ca2+、HCO3-、Br- |
考点:离子共存问题
专题:离子反应专题
分析:根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应,不能相互促进水解反应等,则离子大量共存,以此来解答.
解答:
解:A.H+与ClO- 形成弱酸,不能大量共存,I-与ClO-发生氧化还原反应,不能大量共存,故A错误;
B.Fe3+与OH-反应生成Fe(OH)3,不能大量共存,故B错误;
C.Al3+与AlO2-发生相互促进水解而不能大量共存,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
B.Fe3+与OH-反应生成Fe(OH)3,不能大量共存,故B错误;
C.Al3+与AlO2-发生相互促进水解而不能大量共存,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评:本题考查离子的共存,为高频考点,把握常见离子的反应为解答的关键,侧重复分解、氧化还原反应、相互促进水解反应的离子共存考查,题目难度不大.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
揭示下列变化的离子方程式正确的是( )
| A、明矾用于净水:Al3++3H2O═Al(OH)3↓+3H+ |
| B、钢铁吸氧腐蚀的负极反应:Fe-3e-═Fe3+ |
| C、向明矾溶液中加入少量氢氧化钡溶液:Al3++SO42-+Ba2++3OH-═BaSO4↓+Al(OH)3↓ |
D、苯酚钠饱和溶液中通入少CO2: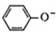 +CO2+H2O→ +CO2+H2O→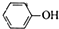 +HCO3- +HCO3- |
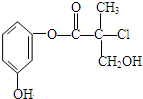 某有机物A是农药生产中的一种中间体,其结构简式如下图.则下列叙述正确的是( )
某有机物A是农药生产中的一种中间体,其结构简式如下图.则下列叙述正确的是( )| A、有机物A属于芳香烃 |
| B、1molA和足量的NaOH溶液反应,最多可以消耗4mol NaOH |
| C、有机物A和浓硫酸混合加热,可以发生消去反应 |
| D、有机物A可以和Br2的CCl4溶液发生加成反应 |
将Cl2通入100mL NaOH溶液中充分反应,生成0.1mol的NaCl,下列说法正确的是( )
| A、反应后溶液中ClO-的个数为0.1NA |
| B、原NaOH浓度为1mol/L |
| C、参加反应的氯气分子为0.1NA |
| D、转移电子为0.2NA |
纳米Cu2O是一种用途广泛的光电材料,可用如下两种电化学装置制备这种材料,下列有关说法中正确的是( )


| A、阳极上的电极反应均为2Cu-2e-+2OH-═Cu2O+H2O |
| B、工作过程中两个装置内溶液的pH均减小 |
| C、两个装置内阴离子均移向铜电极 |
| D、阴极上开始时均有氢气生成 |
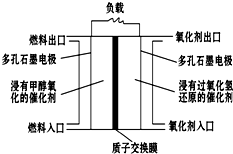 如图是甲醇/过氧化氢燃料电池内部结构示意图.工作时,甲醇和过氧化氢分别进入燃料电池的燃料腔和氧化剂腔,在各自催化剂的作用下发生反应,并向外界输出电能.下列说法不正确的是( )
如图是甲醇/过氧化氢燃料电池内部结构示意图.工作时,甲醇和过氧化氢分别进入燃料电池的燃料腔和氧化剂腔,在各自催化剂的作用下发生反应,并向外界输出电能.下列说法不正确的是( )| A、该电池的正极反应式:H2O2+2H++2e-═2H2O |
| B、燃料腔中的多孔石墨电极为该燃料电池的负极,负极产生的H+通过质子交换膜流向正极 |
| C、电池工作时,1mol甲醇被氧化有6 mol电子转移 |
| D、电路中的电子经正极、负极、质子交换膜后再回到正极,形成闭合回路 |
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、常温下,pH=7的任何溶液中含有OH-数目均为10-7NA |
| B、23g乙醇中含有C-H键的数目为3NA |
| C、4.8g O2和O3以任何比例组成的混合气体中含有的氧原子数目均为0.3NA |
| D、常温常压下,2.24L Cl2与足量铁粉充分反应,转移的电子数目为0.2NA |