题目内容
下列分子的空间构型为平面正三角形的是( )
| A、PCl3 |
| B、BCl3 |
| C、NH3 |
| D、CH2O |
考点:判断简单分子或离子的构型
专题:化学键与晶体结构
分析:立体构型为平面三角形的分子应含有3个δ键,且没有孤对电子,中心原子为sp2杂化,据此分析解答.
解答:
解:A.PCl3中P形成3个δ键,孤对电子数为
(5-3×1)=1,为sp3杂化,含有一个孤对电子,立体构型为三角锥形,故A不选;
B.BCl3中B形成3个δ键,孤对电子数为
(3-3×1)=0,为sp2杂化,立体构型为平面正三角形,故B选;
C.NH3中N形成3个δ键,孤对电子数为
(5-3×1)=1,为sp3杂化,含有一个孤对电子,立体构型为三角锥形,故C不选;
D.CH2O的结构为H-
-H,立体构型为平面三角形,由于三个共价键键长不同,所以不是正三角形,故D不选;
故选B.
| 1 |
| 2 |
B.BCl3中B形成3个δ键,孤对电子数为
| 1 |
| 2 |
C.NH3中N形成3个δ键,孤对电子数为
| 1 |
| 2 |
D.CH2O的结构为H-
| ||
| C |
故选B.
点评:本题考查分子或离子的构型的判断,题目难度中等,注意判断中心原子的价层电子对以及孤对电子数的判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
奥运会禁止运动员使用兴奋剂.以下两种兴奋剂的结构分别为

则关于它们的说法中正确的是( )

则关于它们的说法中正确的是( )
| A、两种兴奋剂均属于芳香烃 |
| B、两种分子中的所有原子均可能共平面 |
| C、利尿酸分子中有三种含氧官能团,有六种氢原子 |
| D、1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br2 |
标准状况下,向100mL FeCl3溶液中通入a L的H2S气体恰好完全反应后,再加入足量的铁粉充分反应.所得溶液经测定金属阳离子的浓度为3mol/L,若反应过程中溶液体积不变,则原FeCl3溶液的物质的量浓度为( )
| A、1 mol/L |
| B、1.5mol/L |
| C、2 mol/L |
| D、以上答案均不正确 |
①、②是两种常见烃的球棍模型,下列对于其共同点的叙述正确的是( )
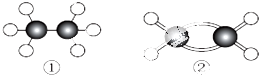

| A、都含有共价键 |
| B、都能发生加聚反应 |
| C、都能发生加成反应 |
| D、等质量的①、②完全燃烧时,放出等质量的CO2 |
从纤维素的化学成分看,它是一种( )
| A、二糖 | B、多糖 | C、酯 | D、脂肪 |
以下事实可充分说明某晶体是原子晶体的是( )
| A、固态时不导电 |
| B、硬而脆 |
| C、无延展性 |
| D、具有空间网状的微观结构 |
下列有关离子化合物的说法正确的是( )
| A、离子化合物一定易溶于水 |
| B、离子化合物由非金属元素和金属元素共同组成 |
| C、熔融状态下能够导电的物质,一定是离子化合物 |
| D、离子化合物在晶体状态下有离子存在,但不导电 |
下列说法不正确的是( )
| A、正戊烷、异戊烷、新戊烷的沸点依次降低 |
| B、17g羟基(-OH)所含有的电子数是9NA |
| C、4.2g C3H6中含有的碳碳双键数一定为0.1NA |
| D、标准状况下,11.2L一氯甲烷所含分子数为0.5NA |