题目内容
19.聚苯乙烯塑料在生产、生活中有广泛应用,其单体苯乙烯可由乙苯和二氧化碳在一定条件下发生如下反应制取: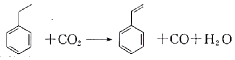
下列有关苯乙烯的说法正确的是( )
| A. | 分子中含有4个碳碳双键 | B. | 属于不含极性键的共价化合物 | ||
| C. | 分子式为C8H10 | D. | 通过加聚反应生成聚苯乙烯 |
分析 苯乙烯中含有碳碳双键和苯环,具有苯、烯烃的性质,能发生加成反应、氧化反应、还原反应、加聚反应,以此解答该题.
解答 解:A.苯乙烯中只有乙烯基含有碳碳双键,苯不含碳碳双键,则分子中含有一个碳碳双键,故A错误;
B.苯乙烯中C-H原子之间存在极性键,故B错误;
C.苯乙烯的分子式为分子式为C8H8,故C错误;
D.苯乙烯中含有碳碳双键,所以能发生加聚反应生成聚苯乙烯,故D正确;
故选D.
点评 本题考查有机物结构和性质,明确官能团与性质关系即可解答,侧重考查基本概念、烯烃、基本反应类型、化学键等知识点,题目难度不大.

练习册系列答案
相关题目
10.对于反应:S(g)+Cl2(g)?SCl2 (g)△H<0,下列措施中能增大正反应速率且平衡常数不变的是( )
| A. | 通入大量的Cl2 | B. | 增大容器容积 | C. | 移去部分SCl2 | D. | 升高温度 |
10.A、B两种元素的原子当它们分别获得两个电子形成惰性元素的电子层结构时,A放出的能量大于B;C、D两元素的原子,当它们分别失去一个电子也形成惰性元素的电子层结构时,吸收的能量D大于C,则A、B和C、D间分别形成离子化合物可能性最大的是( )
| A. | C2A | B. | C2B | C. | D2A | D. | D2B |
7.下列各组中两种物质作用时,反应条件或反应物用量改变,对生成物没有影响的是( )
| A. | Na与O2 | B. | Fe与Cl2 | C. | Fe与稀硝酸 | D. | NaOH溶液与CO2 |
14. “长征”火箭发射使用的燃料是偏二甲肼 (C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼 (C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
 “长征”火箭发射使用的燃料是偏二甲肼 (C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼 (C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )| A. | 从a口通入四氧化二氮气体 | |
| B. | 从d口排除的是NO气体 | |
| C. | H+由A流向B | |
| D. | A极发生的电极反应式:C2H8N2-16e-+8H2O=CO2+N2+16H+ |
4.下列说法正确的是( )
| A. | 用过滤法除去Fe(OH)3胶体中的FeCl3 | |
| B. | Cl2的水溶液能导电,所以Cl2是电解质 | |
| C. | 在蔗糖中加入浓H2SO4后出现发黑现象,说明浓H2SO4具有脱水性 | |
| D. | 向盛有碘水的试管中,加入一定量苯充分振荡后静置,可观察到上层液体几乎无色,下层液体为紫色 |
11.下列说法正确的是( )
| A. | 稀醋酸中加入少量醋酸钠固体能增大醋酸的电离程度 | |
| B. | 室温下,氨水加水稀释后,溶液中c(NH4+)•c(OH-)变大 | |
| C. | NaHCO3溶液中溶质的电离方程式为NaHCO3=Na++H++CO32- | |
| D. | 强电解质溶液导电能力不一定强于弱电解质溶液 |
8.胶体最本质的特征是( )
| A. | 丁达尔效应 | |
| B. | 可以通过滤纸 | |
| C. | 布朗运动 | |
| D. | 分散质粒子的直径在10-9~10-7 m之间 |
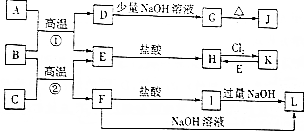
 ;
;