题目内容
正确书写下列化学反应的离子方程式
(1)Cl2和石灰乳的反应:
(2)把H2SO4、Na2SO3、Na2S三种溶液混合:
(3)向漂白粉溶液中通入少量SO2气体:
(4)工业制粗硅的化学方程式:
(5)将盐酸滴入Fe(NO3)2溶液中: .
(1)Cl2和石灰乳的反应:
(2)把H2SO4、Na2SO3、Na2S三种溶液混合:
(3)向漂白粉溶液中通入少量SO2气体:
(4)工业制粗硅的化学方程式:
(5)将盐酸滴入Fe(NO3)2溶液中:
考点:离子方程式的书写
专题:离子反应专题
分析:(1)Cl2和石灰乳的反应生成氯化钙、次氯酸钙和水;
(2)把H2SO4、Na2SO3、Na2S三种溶液混合发生反应生成硫和水;
(3)向漂白粉溶液中通入少量SO2气体反应生成硫酸钙、氯化氢和次氯酸;
(4)二氧化硅与焦炭在高温反应生成硅和一氧化碳;
(5)盐酸滴入Fe(NO3)2溶液反应生成一氧化氮、水、三价铁离子.
(2)把H2SO4、Na2SO3、Na2S三种溶液混合发生反应生成硫和水;
(3)向漂白粉溶液中通入少量SO2气体反应生成硫酸钙、氯化氢和次氯酸;
(4)二氧化硅与焦炭在高温反应生成硅和一氧化碳;
(5)盐酸滴入Fe(NO3)2溶液反应生成一氧化氮、水、三价铁离子.
解答:
解:(1)Cl2和石灰乳的反应生成氯化钙、次氯酸钙和水,离子方程式为:2Cl2+2Ca(OH)2═2Ca2++2Cl-+2ClO-+2H2O;
故答案为:2Cl2+2Ca(OH)2═2Ca2++2Cl-+2ClO-+2H2O;
(2)把H2SO4、Na2SO3、Na2S三种溶液混合发生反应生成硫和水,离子方程式为:2S2-+SO32-+6H+═3S↓+3H2O;
故答案为:2S2-+SO32-+6H+═3S↓+3H2O;
(3)向漂白粉溶液中通入少量SO2气体反应生成硫酸钙、氯化氢和次氯酸,离子方程式为:Ca2++3ClO-+SO2+H2O═CaSO4↓+Cl-+2HClO;
故答案为:Ca2++3ClO-+SO2+H2O═CaSO4↓+Cl-+2HClO;
(4)二氧化硅与焦炭在高温反应生成硅和一氧化碳,化学方程式为:SiO2+2C
Si+2CO↑;
故答案为:SiO2+2C
Si+2CO↑;
(5)将盐酸滴入Fe(NO3)2溶液中,离子方程式为:3Fe2++4H++NO3-═3Fe3++NO+2H2O;
故答案为:3Fe2++4H++NO3-═3Fe3++NO+2H2O.
故答案为:2Cl2+2Ca(OH)2═2Ca2++2Cl-+2ClO-+2H2O;
(2)把H2SO4、Na2SO3、Na2S三种溶液混合发生反应生成硫和水,离子方程式为:2S2-+SO32-+6H+═3S↓+3H2O;
故答案为:2S2-+SO32-+6H+═3S↓+3H2O;
(3)向漂白粉溶液中通入少量SO2气体反应生成硫酸钙、氯化氢和次氯酸,离子方程式为:Ca2++3ClO-+SO2+H2O═CaSO4↓+Cl-+2HClO;
故答案为:Ca2++3ClO-+SO2+H2O═CaSO4↓+Cl-+2HClO;
(4)二氧化硅与焦炭在高温反应生成硅和一氧化碳,化学方程式为:SiO2+2C
| ||
故答案为:SiO2+2C
| ||
(5)将盐酸滴入Fe(NO3)2溶液中,离子方程式为:3Fe2++4H++NO3-═3Fe3++NO+2H2O;
故答案为:3Fe2++4H++NO3-═3Fe3++NO+2H2O.
点评:本题考查了离子方程式的书写,题目难度不大,熟悉反应的实质是解题关键,注意离子方程式遵循质量守恒、电荷守恒定律.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
水的状态除了气、液和固态外,还有玻璃态.它是由液态水急速冷却到165K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
| A、水由液态变为玻璃态,体积缩小 |
| B、水由液态变为玻璃态,体积膨胀 |
| C、玻璃态是水的一种特殊状态 |
| D、玻璃态水是分子晶体 |
在100mL某混合溶液中,c(HNO3)=0.2mol?L-1,c(H2SO4)=0.1mol?L-1,向其中加入1.92g Cu粉,微热充分反应后溶液中的c(Cu2+)为( )
| A、0.15 mol?L-1 |
| B、0.3 mol?L-1 |
| C、0.225 mol?L-1 |
| D、无法计算 |
能用H++OH-=H2O来表示的化学反应是( )
| A、Ba(OH)2溶液滴入稀硝酸中 |
| B、NaHSO4溶液和澄清石灰水反应 |
| C、氢氧化镁和稀盐酸反应 |
| D、二氧化碳通入NaOH溶液中 |
下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为( )
| A、蒸馏水、氨水、氢氧化钡、二氧化硫 |
| B、纯盐酸、空气、硫酸、干冰 |
| C、胆矾、盐酸、铁、碳酸钙 |
| D、氧化钙、漂白粉、氧化铝、碳酸钠 |
钾长石的主要成分为硅酸盐,由前20号元素中的四种组成,化学式为XYZ3W8,其中只有W显负价.X、Y的最外层电子数之和与Z的最高正价数相等,Y3+与W的阴离子具有相同的电子层结构,X、W的质子数之和等于Y、Z的质子数之和.下列说法错误的是( )
| A、X的离子半径>Y的离子半径 |
| B、Z的氢化物稳定性>W的氢化物稳定性 |
| C、化合物X2W2和Y2W3中都不含配位键 |
| D、1mol ZW2晶体所含Z-W键的数目为4NA |
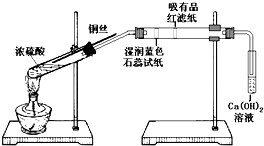 某同学利用如图装置进行浓硫酸和铜反应并验证二氧化硫的性质.按如图实验装置连接仪器和放置药品.加热浓硫酸约1分钟后撤去酒精灯,将铜丝插入液面,反应一段时间后拔出.实验结束后会看到两个试管的液体底部均有少量的白色固体.下列对该实验的现象分析或推断正确的是( )
某同学利用如图装置进行浓硫酸和铜反应并验证二氧化硫的性质.按如图实验装置连接仪器和放置药品.加热浓硫酸约1分钟后撤去酒精灯,将铜丝插入液面,反应一段时间后拔出.实验结束后会看到两个试管的液体底部均有少量的白色固体.下列对该实验的现象分析或推断正确的是( )| A、湿润的蓝色石蕊试纸先变红后褪色 |
| B、左边试管出现的白色固体是由于浓硫酸的脱水性所致 |
| C、从该实验的描述中可以体会出铜与浓硫酸的反应是一个放热反应 |
| D、本实验体现出了二氧化硫的酸性、漂白性和弱氧化性 |