题目内容
10.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 7.8gNa2O2固体中含离子总数为0.4NA | |
| B. | 2.0gH218O和D216O的混合物中所含中子数为NA | |
| C. | 常温下,22.4LCH4中含C-H共价键数为4NA | |
| D. | 标准状况下,11.2LCCl4中含有的分子数为0.5NA |
分析 A、求出过氧化钠的物质的量,然后根据1mol过氧化钠中含2个钠离子和1个过氧根来分析;
B、H218O和D216O的摩尔质量均为20g/mol,且均含10个中子;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、标况下四氯化碳为液体.
解答 解:A、7.8g过氧化钠的物质的量为0.1mol,而1mol过氧化钠中含2个钠离子和1个过氧根,故0.1mol过氧化钠含0.3NA个离子,故A错误;
B、H218O和D216O的摩尔质量均为20g/mol,故2.0g混合物的物质的量为0.1mol,且两者均含10个中子,故0.1mol混合物中含NA个中子,故B正确;
C、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L甲烷的物质的量小于1mol,则含有的C-H键小于4NA个,故C错误;
D、标况下四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量和分子个数,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
20.W、X、Y、Z均为的短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、4、8、8,它们的最外层电子数之和为18.下列说法错误的是( )
| A. | 四种元素一定都是非金属元素 | |
| B. | 常见化合物XZ4分子中只含极性共价键 | |
| C. | 单质的沸点:W>Y | |
| D. | 最高价氧化物的水化物的酸性:Y<Z |
5.化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3,其结构简式如图: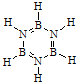 ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:
(1)与(HB=NH)3互为等电子体的分子为C6H6(填分子式).
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中共有4个硼原子,4个氮原子.
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷.工业上采用LiAlH4和BF3,在乙醚介质中反应制得乙硼烷(B2H6),同时生成另外两种产物,该反应的化学方程式为3LiAlH4+4BF3$\frac{\underline{\;乙醚\;}}{\;}$2B2H6+3LiF+3AlF3.
(4)相关化学键的键能如表所示,简要分析和解释下列事实.
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化物,其原因为B-O键键能大于B-B键和B-H键,所以更易形成稳定性更强的B-O键.
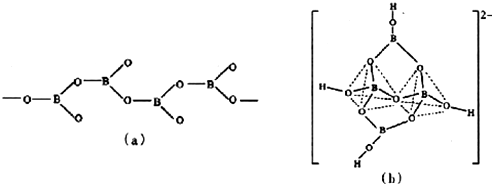
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图(a)为一种无限长单链状结构的多碰酸根,其化学式为BO2-;图(b)为硼砂晶体中的阴离子,其中硼原子采取的杂化类型sp2、sp3.
 ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:(1)与(HB=NH)3互为等电子体的分子为C6H6(填分子式).
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中共有4个硼原子,4个氮原子.
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷.工业上采用LiAlH4和BF3,在乙醚介质中反应制得乙硼烷(B2H6),同时生成另外两种产物,该反应的化学方程式为3LiAlH4+4BF3$\frac{\underline{\;乙醚\;}}{\;}$2B2H6+3LiF+3AlF3.
(4)相关化学键的键能如表所示,简要分析和解释下列事实.
| 化学键 | B-H | B-O | B-B |
| 键能(KJ•mol-1) | 389 | 561 | 293 |
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图(a)为一种无限长单链状结构的多碰酸根,其化学式为BO2-;图(b)为硼砂晶体中的阴离子,其中硼原子采取的杂化类型sp2、sp3.

15.用括号内试剂及操作方法除去下列各物质中的少量杂质,不正确的是( )
| A. | 溴苯中的溴单质(NaOH溶液、分液) | B. | 硝基苯中的苯(蒸馏) | ||
| C. | 乙醇中的水(CaO、蒸馏) | D. | 乙烷中的乙烯(酸性高锰酸钾溶液) |
19.据报道,1995年化学家合成了一种分子式为C200H200的有机物,它是含多个碳碳叁键(-C≡C-)的链状烃,则分子中含碳碳叁键最多是( )
| A. | 49个 | B. | 50个 | C. | 51个 | D. | 不能肯定 |
20.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 将0.1mol•L-1Na2CO3溶液与0.1mol•L-1NaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) | |
| C. | 将0.1mol•L-1NH4Cl溶液与0.1mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| D. | 将0.1mol•L-1Na2C2O4溶液与0.1mol•L-1HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
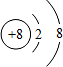 ,DE2的电子式
,DE2的电子式 .
.
 某烃的分子式为C6H10,用热的KMnO4溶液氧化后得到HOOCCH2CH2CH2CH2COOH,由此推断该烃的结构可能的结构简式:
某烃的分子式为C6H10,用热的KMnO4溶液氧化后得到HOOCCH2CH2CH2CH2COOH,由此推断该烃的结构可能的结构简式: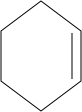 .
.